La psicosis que nos espera
Os dejo aquí un interesante y preocupante editorial de Science. Habla de un problema del que aún no hay información, la coexistencia entre la gripe y la covid. Porque ya sabemos que la gripe comenzará allá por octubre-noviembre como todos los años, y es preocupante saber cómo afectará este hecho con la actual pandemia de covid (que recordemos sigue creciendo a nivel mundial en cuanto al número de nuevos casos diarios).Y es especialmente preocupante el miedo y la psicosis que pueda levantar esta coexistencia gripe-covid en la población (añadiendo también los resfriados comunes). Cuando veamos en cada esquina gente con síntomas gripales o catarrales y sepas que el coronavirus también anda por ahí la sensación será de pánico e inquietud (estrés) constante (más aún cuando la gripe alcance su pico en enero-febrero). Cualquier persona con síntomas va a ser creo, literalmente un "apestado". Las bajas laborales por resfriado común y gripe serán la norma (cuando antes eran la excepción). Es posible, además, que el consumo se relaje mucho en otoño e invierno de nuevo, esta vez posiblemente debido a mini-confinamientos autoimpuestos por una población aterrada. Incluso sin una segunda oleada covid demasiado fuerte.Y por otra parte está el miedo de la propia persona que presenta síntomas. "¿Tendré coronavirus?", será la pregunta que todos los acatarrados y personas con gripe se harán: las consultas ambulatorias (y hospitales) se verán desbordadas posiblemente desde octubre con cientos de miles de personas exigiendo que les hagan un PCR...y repitiendo a los pocos días si los síntomas no mejoran, a sabiendas de que los falsos negativos son posible (y probables al inicio de la infección). Si ya en años previos "normales" la gripe estacional casi lograba ella sola medio colapsar los recursos sanitarios en toda España (recordad esos telediarios mostrando a la gente en camas en los pasillos del hospital); la entrada del covid en escena, junto con la paranoia psicológica y el miedo, conseguirán casi con toda probabilidad que vivamos de nuevo situaciones de colapso similares (o peores) a las de marzo de este año:Peregrinación de centro en centro cuando falten PCR en algunos lugares; gente sintomática con gripe, catarro y covid (y otras patologías distintas) juntas en el mismo lugar pidiendo atención médica e intercambiando gérmenes. Un caos, vaya.Un importante foco de ansiedad estará presente en todos los trabajadores que estén cara al público: dependientes, camareros, etc. Por no hablar de la situación en las residencias de mayores, donde los trabajadores acabarán la mayoría pidiendo la baja por estrés, ansiedad y depresión ante la situación de terror ocurrida cuando la mayor parte de los abuelos presenten síntomas (como todos los años). Y no hablemos ya de los colegios: padres (y profesores) inquietos y recelosos de cualquier niño con mocos. Peleas entre progenitores defendiendo que sus hijos no tienen covid sino resfriado. Familias que no pueden permitirse tener al niño en casa cada vez que presente algún síntoma catarral porque trabajan, ocultando o minimizando por tanto esos síntomas, etc.Queda por delante un otoño-invierno que acabará en los anales de la historia...independientemente de que la segunda oleada covid sea fuerte o no.
Ese día piensa en mí (Los Suaves)
Ese día piensa en mí (Los Suaves):El día que se acabe el tiempo,cuando el sol se apague para mí.El día de la eterna noche sin sueños,cuando por fin deje de sufrir.El día en que de madrugada la damame visite al fin...Ese día piensa en mí.Descansaré en paz, amigo.Calla, no llores por mí.He escogido mi camino.El día sin luz anterior a mi entierro,cuando las moscas se posen en mí.El día en que nadie cierre mis ojosy que ni una lágrima corra por mí.El día que veas que mi miradano se fija en ti...Ese día piensa en mí.Descansaré en paz, amigo.Calla, no llores por mí.He escogido mi camino.Ese día piensa en mí.Descansaré en paz, amigo.Calla, no llores por mí.He escogido mi camino.El día en que se acaben los recuerdos,cuando la muerte me encuentre por fin.El día en que llega el gran desengaño,cuando la vida se burla de ti.El día en que sepa que no soy naday nada hay para míEse día piensa en mí.Descansaré en paz, amigo.Calla, no llores por mí.He escogido mi camino.
Cuando la evolución decide quién vive
En la, de momento, primera ola de la actual pandemia de coronavirus; no sólo España sino otros muchos países tuvieron que decidir en pleno pico de contagios y a las puertas del colapso sanitario cómo priorizar las camas hospitalarias y las plazas UCI disponibles. En concreto, mayormente se dio prioridad (en caso de necesidad de elegir) a las personas más jóvenes frente a las mayores, llegándose a casos en que directamente se prohibió el traslado de mayores de 75 años a los hospitales.Y es ahora, a toro pasado, cuando vienen los debates; con fines políticos e ideológicos casi siempre, sobre la ética o falta de ética de aquellas decisiones tomadas en plena escalada, cuando simple y llanamente no había recursos médicos para todos. Pero cualquiera con dos dedos de frente puede ver que la determinación de "salvar" a los jóvenes sobre los "viejos" no fue para nada algo racional, sino un proceso instintivo (casi un acto espontáneo que siguieron -y siguen- a pies juntillas gobiernos de derecha y de izquierda por igual).Porque lo mismo que dice esa ley no escrita por la que ante un naufragio tienen siempre preferencia los niños y las embarazadas, existen muchas otras leyes naturales (instintivas e innatas) que nos son desconocidas hasta que desgraciadamente llega el momento de tener que optar por una opción mala u otra peor. En el caso de esta inusual pandemia nos vimos de repente con el requerimiento de decidir cómo priorizar los escasos recursos médicos: ¡y la evolución decidió por nosotros, por supuesto! Simplemente, y de manera natural (automática), todos los que se vieron en la necesidad de realizar tal selección (no todas las comunidades ni todos los países se vieron desbordados por igual) sin excepción antepusieron la vida de los más jóvenes sobre la de los más ancianos.Y esto fue así porque simple y llanamente la evolución de manera instintiva nos hace tender a ayudar y asistir con más ímpetu a aquellos individuos que tienen más "valor" evolutivo (replicativo) por delante. Las personas en edad reproductiva (o que aún no alcanzaron dicha edad) siempre son naturalmente "preferibles" a las personas que ya casi finalizaron su "misión" natural evolutiva.Ésto desde luego en lo relativo al sujeto parece un acto natural cruel, pero debemos recordar que objetivamente en la naturaleza no hay nada Bueno ni Malo (con mayúsculas). No es malo el león ni buena la gacela. Ni es mala una bacteria que mata una persona. Tampoco es bueno ni malo el médico o dirigente político que instintivamente se ve "forzado" a anteponer la vida del joven sobre la de la persona mayor: es tan sólo algo natural. Y si alguien se siente tentado de culpar a alguien, que culpe al modo en que funciona esencialmente el mundo evolutivo o, si es creyente, que culpe a su Dios.
Una reflexión tras más de 60 días de confinamiento
Vivimos en el peor mundo imaginable: uno que permite la existencia de seres conscientes del sinsentido objetivo de su ser, y que además se ven forzados a luchar con vehemencia (cuales somas desechables o marionetas de pacotilla) por esos "fines" (termodinámicos) inútiles en lo relativo al sujeto.Pero no te preocupes si estas palabras racionalmente te incomodaron por un instante, puesto que tenemos un sesgo evolutivo que se encargará pronto de darte consuelo: portamos, inscrito a fuego en los "circuitos" neuronales de nuestro cerebro, un instintivo pensamiento mágico-optimista que hacen olvidar pronto este tipo de revelaciones, y que se encarga de facilitar la vuelta a la "normalidad" emocional. Este sesgo se bastará para permitirte continuar con tu día normalmente; movido por esos invisibles hilos físicos que te guían desde el mismo momento de tu nacimiento. La posible disonancia cognitiva que haya podido aparecer a tu conciencia se esfumará de tu mente casi de inmediato, y de este modo podrás volver a tus (necios) quehaceres diarios en un abrir y cerrar de ojos.Por lo tanto nos dejamos llevar con la idea de que todo está bien. Y ciertamente todo está bien...hasta que tarde o temprano el velo del engaño instintivo cruelmente se deja caer. Quizás no hoy, ni mañana; pero es cuestión de tiempo: en algún momento, quizás unos instantes antes de morir en un accidente de tráfico, o cuando un médico nos diagnostique una pronta muerte, lo mismo da; será precisamente cuando caiga el telón y te veas como un bobo: como esa estúpida marioneta con aires de grandeza que siempre has sido. La Naturaleza (sea eso lo que sea) se aprovechó de ti, pero no te dejará entenderlo justo hasta ese momento, cuando hayas pasado de soma desechable, a ya un soma desechado. Al perder la utilidad práctica, el mundo te permitirá echar un rápido vistazo a la verdadera realidad encubierta...y entonces de una patada te enviará a la nada de la que fuiste engendrado.Más pronto que tarde todos, sin excepción; veremos por fin que fuimos manejados, usados...consumidos. El mundo natural nos utilizó, quién sabe esencialmente para qué, obligándonos en todo momento a movernos del modo adecuado, cual roca que debe caer cuando se la deja rodar desde lo alto de la colina. Pero durante nuestro trayecto vital este hecho sádicamente se nos ocultó (naturalmente) para que no fuese un impedimento ante nuestra ingrata, espontánea y subjetivamente inútil tarea termodinámica de degradar gradientes (producir, consumir, producir, consumir,...). Sin embargo, insistamos de nuevo, de manera más o menos inefable todos lo acabaremos por comprender algún día: no somos más, como individuos y como sociedad, que el equivalente dinámico de cualquier otro movimiento físico, con la excepción de la complejidad y de los grados en la libertad de acción: una piedra que tras caer, se las ingenia para subir de nuevo al monte y repetir espontáneamente este ciclo una infinidad de veces, o al menos, mientras el mundo aguante en pie.Sísifo estaría feliz de descubrir que su castigo es el castigo del hombre. Una felicidad desquiciada por el conocimiento del absurdo, claro está.
Los cuatro factores (aún desconocidos) que van a determinar el futuro "sano" de nuestra civilización
Hay ahora mismo cuatro factores (de momento desconocidos) que van a determinar literalmente el futuro "sano" de nuestra civilización tal y como la conocemos:1) Conocer cuánto dura la inmunidad (memoria) hacia el SARS-CoV-2 y cuánta seroprevalencia existe actualmente (lo que determinará la relación infectados/muertos: letalidad, y lo lejos o cerca que estamos de la inmunidad de grupo). También conocer si esta inmunidad adquirida es eficiente y suficiente para no volver a infectarse del virus aunque sea de manera más leve.2) Cómo afecta los cambios de temperatura y humedad al virus.3) Conocer si es posible realizar una vacuna eficiente, barata y fácil de producir en masa; y de ser posible, para cuándo estaría al alcance de 7.000 millones de personas.4) Determinar si la tasa de mutación de este virus de ARN monocatenario positivo, una vez se vea bajo presión evolutiva (ya sea debido a que se logre vacuna o inmunidad de grupo "natural"), le permitirá safarse con facilidad o no de esta barrera inmune creando nuevas cepas o cambios significativos (como es capaz de hacer la gripe, por ejemplo, o incluso otros coronavirus hermanos, de cuyos resfriados no se libra casi nadie año tras año por mucho que se inmunice la gente de ellos).
Jarro de agua fría sobre la seroprevalencia. Este estudio indica datos que no superan el 5% casi en ninguna comunidad autónoma (la media nacional está alrededor del 2%). Recordemos que la inmunidad de grupo (o "rebaño") se alcanza cuando se alcanza algo así como un 70%-80% aproximadamente (el rango exacto varía según el virus pero para el SARS-CoV-2 no se espera que baje del 65% ni en las estimaciones más optimistas). Esto implica que hemos contenido el virus "demasiado" bien y que la población susceptible de ser infectada aún es de casi el 98% (según zonas).
La actual "desescalada" en estas circunstancias es muy peligrosa, por no decir suicida (más aún si finalmente el factor ambiental afecta al virus menos de lo esperado, cosa que no se puede descartar de momento).
#3 Mas preocupante es que antes de llegar a dicho porcentaje los primeros infectados es posible que ya no sean inmunes, lo que suena a broma cruel.
#4 Parece que han confirmado que no es posible.
https://www.larazon.es/salud/20200502/3ytnddo2yvaj7bnya4hrgdvbe4.html
#9 no pueden recontagiarse ahora. Ninguna fuente que leas te va a decir que dicha inmunidad durara mas de dos anyos
#12 teniendo en cuenta que se necesita mucho mas de dos anyos para llegar a niveles razonables, no. Si aceleras el proceso saturas el sistema sanitario y viviriamos socialmente en un infierno tan grande que la gente tampoco gastaria y la economia tampoco funcionaria.
La respuesta es la ciencia, que se encuentren tratamientos y ojala una vacuna. Lo malo es que nadie puede prometer plazos ni exito, es en resumen una gran mierda. Yo soy de los "a priori" y ni asi imagine que un virus con tan poca letalidad danyara a la sociedad tan eficientemente.
#9 el titular no dice lo que dice la noticia. El estudio de los surcoreanos habla de que los que volvieron a dar positivo fue por errores en los test. No habla en ningún caso del tiempo de inmunidad. Ni si quiera habla de cómo funciona la inmunidad con respecto a diferentes cepas. No existe tal estudio.
#4 Informe de expertos predice hasta dos años más de miseria pandémica/c4#c-4
Sí, esa posibilidad también la había contemplado. Lo de aplanar la curva para tener infectado al 70% de la población solo que en un tiempo mucho más largo (hablan de 18-24 meses) puede tener esa contrapartida. Y eso sin necesidad de que el virus haya mutado lo suficiente.
#2 He sido partidario absoluto del confinamiento y tuve dudas de la apertura parcial de la economía hace 2 semanas aunque parece no haber ido mal, creo que el confinamiento si horizonte no es realista es posible que sea algo precipitado pero no creo que la dichosa economía nos permita sostener la situación más , no he visto que pongas ninguna alternativa.
#2 La cifra es muy similar al estudio que se ha llevado a cabo en Francia.
https://www.futura-sciences.com/sante/actualites/coronavirus-coronavirus-6-francais-auront-ete-contamines-ici-11-mai-80654/
Primer estudio que revela la protección de nuestra población ante el coronavirus [CAT]
eapsardenya.catEl EAP Cerdeña ha realizado un estudio transversal de prevalencia poblacional de seropositividad al SARS-CoV-2[...]Se han utilizado muestras de sangre capilar y los test utilizados son test de diagnóstico rápido que permiten detectar IgG e IgM por la técnica de inmunocromatografia de difusión.[...]Un 5,47% de los participantes han mostrado un resultado positivo, siendo en el grupo de hombres un 4,4% y en el grupo de mujeres un 6,4%.
Explicando el famoso paper: "Proyectando la dinámica de transmisión del SARS-CoV-2" (Parte II)
En una entrada anterior comenzamos a explicar uno de los los papers más interesantes y citados en relación a la dinámica presente y futura del SARS-CoV-2. El trabajo en cuestión, desarrollado por investigadores de Harvard se titula: "Proyectando la dinámica de transmisión del SARS-CoV-2 durante el período pospandémico". Tenéis el original aquí, y una traducción al castellano que yo mismo realicé en este mismo blog aquí.El trabajo de estos autores de los departamentos de Inmunología y Enfermedades Infecciosas e Epidemiología de Harvard es a la vez simple y complejo de entender. Es complejo en cuanto a la metodología estadística y los modelos matemáticos utilizados (detalles al alcance de los más expertos en la materia que se recogen en un apartado de materiales complementarios que ya de por sí es casi un paper independiente por lo denso). Pero a la vez es simple en cuanto a lo "sencillo" que es entender los resultados de la aplicación de dichos modelos frente al mundo real.Pues bien. Como decimos, hace unos días ya realizamos el primer acercamiento divulgativo de lo que este ensayo dice. En concreto, nos centramos en la primera sección del paper, donde los investigadores nos hablan de la probable dinámica del virus en en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención alguna.Creo que es casi imprescindible echar un vistazo a esta primera sección antes de continuar con lo que hoy trataremos. En caso contrario, cabe la posibilidad de que no se entienda bien de lo que vamos a hablar a continuación o de que no suscite el interés que realmente creo que merece, puesto que es en esta segunda sección del trabajo donde los investigadores de Harvard proponen los posibles escenarios que podrían llegar a partir del momento que estamos viviendo actualmente. Es decir, aquellos escenarios donde se estudia la dinámica pandémica y pospandémica teniendo en cuenta las medidas de contención disponibles actualmente.De cualquier manera, vamos a repetir los mismos comentarios iniciales que ya hicimos en la entrada anterior:Comentarios iniciales.Es necesario comentar antes de nada un par de cuestiones imprescindibles para poder entender mínimamente la dinámica del SARS-CoV-2:1) El COVID-19 es el nombre que se le ha dado a la enfermedad que causa el virus denominado SARS-CoV-2. Una cosa es la enfermedad (como por ejemplo, el SIDA), y otra el virus que lo causa (en el caso del SIDA es el VIH).2) El virus SARS-CoV-2 es un coronavirus (Orthocoronavirinae). Para la subfamilia del coronavirus existen a su vez cuatro géneros: Alphacoronavirus, Betacoronavirus, Gammacoronavirus y Deltacoronavirus. El SARS-CoV-2 pertenece al género Betacoronavirus.3) Además del SARS-CoV-2, existen muchos otros virus de la subfamilia coronavirus que son capaces de transmitirse de humano a humano. Entre ellos tenemos al MERS-CoV (que produce desde el 2015 la enfermedad aún en activo llamada: síndrome respiratorio de Oriente Medio), el SARS-CoV-1 (que apareció y desapareció entre los años 2002/2003 produciendo la enfermedad: síndrome respiratorio agudo grave), y otros muchos virus que por su levedad cuadran y se aglutinan en lo que se llama resfriado común. Es decir, que eso que nos contagia casi cada año y que denominamos resfriado (enfermedad), es en realidad producto casi siempre de un tipo de los restantes coronavirus capaces de infectar humanos.4) El 15% de los resfriados son causados por coronavirus, y de estos casos, la mayor parte los producen los coronavirus: HCoV-229E, HCoV-NL63, HCoV-0C43 y HCoV-HKU1.5) De entre estos cuatro, sólo dos pertenecen al mismo género Betacoronavirus del SARS-CoV-1, SARS-CoV-2, y el MERS-CoV. Se trata del HCoV-OC43 y el HCoV-HKU1.6) Todos los Betacoronavirus presentan, dada su similitud filogenética, cierta inmunidad cruzada. Se conoce la realidad este proceso gracias al estudio de los coronavirus del resfriado común. Por ejemplo; pasar el HCoV-OC43 te inmuniza hasta cierto punto y tiempo frente al HCoV-HKU1, y viceversa. En el estudio del que estamos hablando se supone, según el escenario, que también existe cierta inmunidad cruzada entre estos virus "del resfriado" y el SARS-CoV-2. Y modelan la dinámica del COVID19 otorgando varios valores a dicho factor de inmunidad cruzada (de más débil a más fuerte).7) Por otra parte, el estudio también basa los escenarios pronosticados a partir de lo que denominan factor estacional. Es decir, cuánto y cómo afecta al virus los climas húmedos y las temperaturas más altas. En este sentido, varían también en las simulaciones que realizan los números para este factor.8) También utilizan, por supuesto, el factor más importante para todo modelo epidemiológico: la inmunidad de grupo. Es decir, cuándo y cómo se alcanzará el punto en que más del 60% de la población deja de ser susceptible al virus (por haber pasado la enfermedad). En este sentido, cobra especial importancia para entender la dinámica futura conocer cuánta inmunidad (anticuerpos) produce nuestro cuerpo tras pasar la infección, y qué "memoria" o duración tienen dichos anticuerpos. En este sentido, y a raíz de lo que se sabe de los virus del resfriado HCoV-OC43 y HCoV-HKU1, proponen que la inmunidad dura entre 40 semanas (en el peor escenario) y 104 semanas (en el mejor caso). La inmunidad permanente la tienen en cuenta, pero se sabe que es un escenario MUY poco probable.9) Finalmente, toman como parámetro para la simulación la intensidad y el momento de las medidas de control que tomen los gobiernos.Simulando la transmisión de SARS-CoV-2.Independientemente de la dinámica de transmisión pospandémica del SARS-CoV-2, se requieren medidas urgentes para abordar la epidemia en curso. Los tratamientos farmacéuticos y las vacunas pueden requerir meses o años para desarrollarse y probarse, dejando las intervenciones no farmacéuticas (NPI) como el único medio inmediato para frenar la transmisión del SARS-CoV-2. Como resultado de ésto, se han adoptado medidas de distanciamiento social en muchos países con transmisión generalizada de SARS-CoV-2.En el paper, el equipo de investigación estudia en su segunda sección los posibles resultados de estas medidas de distanciamiento según varios parámetros. Para ello, parten del modelo matemático SEIRS descrito en la primera sección del trabajo (lo cual ya estudiamos aquí) donde describen la dinámica natural (inalterada) del virus y la adaptan para continuar el estudio suponiendo de partida:- Que el ratio de infecciones moderadas/leves/asintomáticas es del 95.6% del total de infecciones, que las infecciones que conducen a la hospitalización pero no a una atención médica crítica es del 3.08% del total, y que las infecciones que requieren de cuidados intensivos es del 1.32%.- Asumen χ 3X = 0.3, χ X3 = 0, lo cual indica (insisto: ver entrada anterior) que hay muy poca inmunidad cruzada entre los Betacoronavirus del resfriado común y el COVID19. Es decir, que infectarse con los virus HCoV-OC43 y HCoV-HKU1 no implicaría tener mucha menos probabilidad de infectarse por SARS-CoV-2.- Asumen un período latente medio de 4,6 días y un período infeccioso de 5 días (a partir de varios estudios que enlazan a pie de página en el trabajo original).- Asumen una duración media de estancia hospitalaria no crítica de 8 días, y de 6 días para aquellos casos que sí requieren de cuidados intensivos. Toman también que la duración media de dicha atención intensiva es de 10 días.- Por último tienen en cuenta los dos casos de factores ambientales estudiados en la sección anterior. Es decir: f = 0.2, lo cual implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura. Y, f = 0.4, lo que implica alta variación estacional. En este caso, el SARS-CoV-2 se vería bastante afectado por los cambios ambientales de humedad y temperatura.Escenarios de distanciamiento social único.Sabido ésto, ya estamos en condiciones de entender la segunda sección del trabajo original, donde los chicos de Harvard se centran en aquellos escenarios donde los países realizan un único esfuerzo de distanciamiento social. Es decir, nos explican qué ocurriría, según su modelo, en el caso de no poseerse vacunas, tratamientos, y de que los gobiernos no fuesen capaces más que de realizar un único esfuerzo de distanciamiento social efectivo. En otras palabras: si, como está sucediendo actualmente, tras un primer gran confinamiento se abren las puertas (desescalada) para no volver a cerrarlas (por incapacidad económica, política y/o social).Estos serán precisamente los escenarios que vamos a contemplar a continuación variando tres parámetros: el factor ambiental f, el éxito del confinamiento (es decir, lo estricto y eficiente que ha sido el mismo), y el tiempo que se mantiene dicho confinamiento único antes de levantarse de manera más o menos gradual (para el caso es casi lo mismo).Vamos a ver estos escenarios donde, insistamos una vez más, se supone siempre un periodo de distanciamiento social único ("abrir para no cerrar" o "cerrar" pero de manera muy poco eficiente por motivos económicos, políticos o sociales):Nota: todos los escenarios toman el 11 de marzo de 2020 como fecha de inicio de este único período de distanciamiento social.Fijémonos en el escenario A). Si el factor ambiental es poco importante
Si el factor ambiental es poco importante Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (A) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y cuatro semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Y aunque parece una gráfica compleja os aseguro que es muy sencilla de entender:- Se ven 4 líneas de colores sólidas, y 4 líneas de colores punteadas. Las líneas sólidas hacen referencia siempre al número total de casos infecciosos no críticos, mientras que las líneas punteadas hacen referencia a los casos que resultan ser severos y requieren atención médica especializada.- Los colores representan la eficacia del distanciamiento. El color negro implica 0% (es decir, no tomar medida alguna), el rojo implica una eficacia relativa del 20%, el azul una eficacia del 40% y finalmente el verde implica la mayor eficiencia tenida en cuenta: un 60%.¿Qué significa pues este escenario A)?La interpretación es bastante simple:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se hubiese levantado a las 4 semanas después del 11 de marzo (a mediados de abril aproximadamente), para finales de verano aproximadamente habríamos alcanzado la inmunidad de grupo (o de "rebaño") puesto que la mayor parte de la población mundial (integral de la curva) habría pasado la enfermedad, dejando por el camino millones de casos críticos y de muertos. Se observa además poca diferencia en la efectividad del confinamiento (colores) si el mismo se mantiene tan "poco" tiempo (un mes en este caso A).En la segunda figura vemos que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental sí es importante; si el confinamiento se hubiese levantado a las 4 semanas después del 11 de marzo (a mediados de abril aproximadamente), habríamos alcanzado igualmente la inmunidad de grupo (o de "rebaño") puesto que la mayor parte de la población mundial (integral de la curva) pasará la enfermedad, pero en este caso sí que se observa diferencias según la efectividad del confinamiento. A mayor eficacia, mayor aplanamiento de la curva, y más meses pasarán hasta que la pandemia finalice debido a que dejen de existir personas susceptibles de contagiarse (la inmunidad de grupo se estima que se logrará cuando entre el 70% y el 80% de la población tenga anticuerpos para el virus).Nota importante: en el escenario (A), no importa cual sea el factor ambiental, siempre se acaba sobrepasando la capacidad hospitalaria y de recursos médicos en cualquier país, pero de largo. Eso supone millones de muertos. El caso promedio en el mejor caso de la primera figura supone un pico donde el 20% de la población mundial se encuentra infectada al mismo tiempo, en la segunda gráfica, el mejor caso supone que un 5% de la población se encuentra pasando la enfermedad en cierto momento. Estos números implican más de un billón (con b) de infectados (20% de 7.000 millones de personas), o 350 millones (5% de la población mundial). La inmunidad de grupo en este caso (A) supondría un coste en mortalidad de varias decenas o cientos de millones de personas.Fijémonos en el escenario B).
Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (A) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y cuatro semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Y aunque parece una gráfica compleja os aseguro que es muy sencilla de entender:- Se ven 4 líneas de colores sólidas, y 4 líneas de colores punteadas. Las líneas sólidas hacen referencia siempre al número total de casos infecciosos no críticos, mientras que las líneas punteadas hacen referencia a los casos que resultan ser severos y requieren atención médica especializada.- Los colores representan la eficacia del distanciamiento. El color negro implica 0% (es decir, no tomar medida alguna), el rojo implica una eficacia relativa del 20%, el azul una eficacia del 40% y finalmente el verde implica la mayor eficiencia tenida en cuenta: un 60%.¿Qué significa pues este escenario A)?La interpretación es bastante simple:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se hubiese levantado a las 4 semanas después del 11 de marzo (a mediados de abril aproximadamente), para finales de verano aproximadamente habríamos alcanzado la inmunidad de grupo (o de "rebaño") puesto que la mayor parte de la población mundial (integral de la curva) habría pasado la enfermedad, dejando por el camino millones de casos críticos y de muertos. Se observa además poca diferencia en la efectividad del confinamiento (colores) si el mismo se mantiene tan "poco" tiempo (un mes en este caso A).En la segunda figura vemos que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental sí es importante; si el confinamiento se hubiese levantado a las 4 semanas después del 11 de marzo (a mediados de abril aproximadamente), habríamos alcanzado igualmente la inmunidad de grupo (o de "rebaño") puesto que la mayor parte de la población mundial (integral de la curva) pasará la enfermedad, pero en este caso sí que se observa diferencias según la efectividad del confinamiento. A mayor eficacia, mayor aplanamiento de la curva, y más meses pasarán hasta que la pandemia finalice debido a que dejen de existir personas susceptibles de contagiarse (la inmunidad de grupo se estima que se logrará cuando entre el 70% y el 80% de la población tenga anticuerpos para el virus).Nota importante: en el escenario (A), no importa cual sea el factor ambiental, siempre se acaba sobrepasando la capacidad hospitalaria y de recursos médicos en cualquier país, pero de largo. Eso supone millones de muertos. El caso promedio en el mejor caso de la primera figura supone un pico donde el 20% de la población mundial se encuentra infectada al mismo tiempo, en la segunda gráfica, el mejor caso supone que un 5% de la población se encuentra pasando la enfermedad en cierto momento. Estos números implican más de un billón (con b) de infectados (20% de 7.000 millones de personas), o 350 millones (5% de la población mundial). La inmunidad de grupo en este caso (A) supondría un coste en mortalidad de varias decenas o cientos de millones de personas.Fijémonos en el escenario B). Si el factor ambiental es poco importante
Si el factor ambiental es poco importante Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (B) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y ocho semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario B)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados de mayo, fecha muy próxima a lo que los países se encuentran pensando actualmente!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta a las 8 semanas después del 11 de marzo (a mediados de mayo aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 20%): en este caso, se observa un escaso aplanamiento de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Ni siquiera se observa un repunte pronunciado una vez se levantan las medidas de contención.- Línea azul. Eficacia del confinamiento del 40% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 40%): este caso es muy interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero quizás se aproxima a la realidad en el caso de que el factor ambiental sí sea importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo mediados de mayo como fecha límite) tendremos un repunte de casos muy importante que se alargará durante meses hasta alcanzarse la inmunidad de grupo a finales de año.- Línea verde. Eficacia del confinamiento del 60% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 60%): este caso es el más interesante de este escenario. En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme, llevando a la inmunidad de grupo para finales de septiembre tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos porque este escenario no sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (B), entonces el repunte de casos será muy gradual, alcanzando un nuevo pico (que se podría llamar oleada) para mediados de octubre. Este escenario es muy valorado como probable por la mayoría de la comunidad científica. Nota importante: si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (B), lo cual llevaría a dar marcha atrás inmediata, e intentarse retornar al confinamiento estricto (absoluto) al poco tiempo de levantarse el mismo. Es algo que sabremos pronto dado que todos los países tienen planteado levantar el confinamiento paulatinamente durante mayo-junio de este año.Fijémonos en el escenario C).
Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (B) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y ocho semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario B)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados de mayo, fecha muy próxima a lo que los países se encuentran pensando actualmente!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta a las 8 semanas después del 11 de marzo (a mediados de mayo aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 20%): en este caso, se observa un escaso aplanamiento de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Ni siquiera se observa un repunte pronunciado una vez se levantan las medidas de contención.- Línea azul. Eficacia del confinamiento del 40% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 40%): este caso es muy interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero quizás se aproxima a la realidad en el caso de que el factor ambiental sí sea importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo mediados de mayo como fecha límite) tendremos un repunte de casos muy importante que se alargará durante meses hasta alcanzarse la inmunidad de grupo a finales de año.- Línea verde. Eficacia del confinamiento del 60% (técnicamente se supone una reducción artifical de la tasa de infección del virus R0 de un 60%): este caso es el más interesante de este escenario. En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme, llevando a la inmunidad de grupo para finales de septiembre tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos porque este escenario no sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (B), entonces el repunte de casos será muy gradual, alcanzando un nuevo pico (que se podría llamar oleada) para mediados de octubre. Este escenario es muy valorado como probable por la mayoría de la comunidad científica. Nota importante: si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (B), lo cual llevaría a dar marcha atrás inmediata, e intentarse retornar al confinamiento estricto (absoluto) al poco tiempo de levantarse el mismo. Es algo que sabremos pronto dado que todos los países tienen planteado levantar el confinamiento paulatinamente durante mayo-junio de este año.Fijémonos en el escenario C). Si el factor ambiental es poco importante
Si el factor ambiental es poco importante Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (C) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y doce semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario C)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados de junio, fecha todavía más próxima que en el caso (B) a lo que los países se encuentran pensando actualmente!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta a las 12 semanas después del 11 de marzo (a mediados de junio aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20%: en este caso se observa un aplanamiento todavía escaso de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Esto no cuadra con los datos empíricos disponibles.- Línea azul. Eficacia del confinamiento del 40%: este caso es muy interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero se aproxima a la realidad más que en el caso (B) en el caso de que el factor ambiental sí sea importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo mediados de junio como fecha límite) tendremos un repunte de casos gradual pero pronunciado que llevará a un pico (nueva oleada) a mediados de octubre.- Línea verde. Eficacia del confinamiento del 60%: este caso es también el más interesante de este escenario (C). En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme (similar al del escenario B), llevando a la inmunidad de grupo para finales de septiembre tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos porque este escenario tampoco sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (C), entonces el repunte de casos será muy gradual, ¡tan gradual y plano que es peligroso! Los contagios parecen desparecer y muchos pensarán que el virus está bajo control, sin embargo; el factor estacional y la artificial eficacia del confinamiento (que dejará a la mayor parte de la población como susceptible de ser infectada), harían que para principios de octubre aparezca una nueva oleada que probablemente pillaría por sorpresa a gran parte del mundo que estaría en pleno proceso de recuperar la normalidad económica y social en ese momento. Esta segunda oleada, como ya se ha comentado, es el escenario valorado como más probable por la mayoría de la comunidad científica, pero eso no significa que la clase política, la economía, y/o la sociedad estén listas para aceptar las consecuencias que supondría tener que hacer frente de nuevo a una nueva pandemia. Es posible que los gobiernos o la situación geopolítica y social no permitan en octubre nuevos confinamientos estrictos, y la eficacia de las medidas que se tomen podrían bajar en eficacia mucho respecto del actual confinamiento (que es posible que haya superado una eficiencia del 50% rebajando el R0 del virus).Nota importante: de nuevo, si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (C), lo cual llevaría a dar marcha atrás inmediata, e intentarse retornar al confinamiento estricto (absoluto) al poco tiempo de levantarse el mismo. Es algo que sabremos pronto dado que todos los países tienen planteado levantar el confinamiento paulatinamente durante mayo-junio de este año.Fijémonos en el escenario D).
Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (C) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y doce semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario C)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados de junio, fecha todavía más próxima que en el caso (B) a lo que los países se encuentran pensando actualmente!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta a las 12 semanas después del 11 de marzo (a mediados de junio aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20%: en este caso se observa un aplanamiento todavía escaso de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Esto no cuadra con los datos empíricos disponibles.- Línea azul. Eficacia del confinamiento del 40%: este caso es muy interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero se aproxima a la realidad más que en el caso (B) en el caso de que el factor ambiental sí sea importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo mediados de junio como fecha límite) tendremos un repunte de casos gradual pero pronunciado que llevará a un pico (nueva oleada) a mediados de octubre.- Línea verde. Eficacia del confinamiento del 60%: este caso es también el más interesante de este escenario (C). En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme (similar al del escenario B), llevando a la inmunidad de grupo para finales de septiembre tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos porque este escenario tampoco sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (C), entonces el repunte de casos será muy gradual, ¡tan gradual y plano que es peligroso! Los contagios parecen desparecer y muchos pensarán que el virus está bajo control, sin embargo; el factor estacional y la artificial eficacia del confinamiento (que dejará a la mayor parte de la población como susceptible de ser infectada), harían que para principios de octubre aparezca una nueva oleada que probablemente pillaría por sorpresa a gran parte del mundo que estaría en pleno proceso de recuperar la normalidad económica y social en ese momento. Esta segunda oleada, como ya se ha comentado, es el escenario valorado como más probable por la mayoría de la comunidad científica, pero eso no significa que la clase política, la economía, y/o la sociedad estén listas para aceptar las consecuencias que supondría tener que hacer frente de nuevo a una nueva pandemia. Es posible que los gobiernos o la situación geopolítica y social no permitan en octubre nuevos confinamientos estrictos, y la eficacia de las medidas que se tomen podrían bajar en eficacia mucho respecto del actual confinamiento (que es posible que haya superado una eficiencia del 50% rebajando el R0 del virus).Nota importante: de nuevo, si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (C), lo cual llevaría a dar marcha atrás inmediata, e intentarse retornar al confinamiento estricto (absoluto) al poco tiempo de levantarse el mismo. Es algo que sabremos pronto dado que todos los países tienen planteado levantar el confinamiento paulatinamente durante mayo-junio de este año.Fijémonos en el escenario D). Si el factor ambiental es poco importante
Si el factor ambiental es poco importante Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (D) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y veinte semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario D)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados/finales de julio, fecha aún más próxima que la del caso (C) a lo que los países se encuentran actualmente pensando hacer de manera gradual!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta levantado 20 semanas después del 11 de marzo (mediados/finales de julio aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20%: en este caso se observa un aplanamiento todavía escaso de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Esto no cuadra con los datos empíricos disponibles.- Línea azul. Eficacia del confinamiento del 40%: este caso es de nuevo interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero se aproxima mucho más a la realidad que en el caso (C) cuando el factor ambiental sí es importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo finales de julio como fecha límite) tendremos un repunte de casos gradual pero pronunciado que llevará a un pico (nueva oleada) a mediados de octubre.- Línea verde. Eficacia del confinamiento del 60%: este caso es todavía más interesante que en el escenario (C). En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme (similar al del escenario C), llevando a la inmunidad de grupo para finales de año tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos una última vez más porque este escenario tampoco sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (D), entonces el repunte de casos será muy gradual, ¡tan gradual y plano que es muy peligroso! Los contagios parecen desparecer y muchos pensarán que el virus está bajo control (incluso bien entrados ya en octubre, cosa que no sucedía en el caso C). Sin embargo; el factor estacional y la artificial eficacia del confinamiento (que dejará a la mayor parte de la población como susceptible de ser infectada), harían que para principios del año 2021 apareciera súbitamente una nueva oleada que, probablemente, pillaría por sorpresa (más que en el caso C) a gran parte de un mundo en pleno proceso de recuperación de la normalidad económica y social en ese momento. Además, y para más inri, esta nueva oleada se solaparía con la de la gripe estacional. Este escenario más probable del escenario (D) en realidad no es más que una copia del escenario (C) pero con la oleada atrasada un mes y medio. Sin embargo, este retraso podría confiar más aún a la población y a la clase política (necesitada de buenas notificas) pensando que el virus está erradicado, lo cual llevaría posiblemente a un negacionismo y a una relajación (que no detención) ante la búsqueda activa de tratamiento y/o vacunas.Esta segunda oleada "retrasada" (hasta enero del 2021) respecto de lo que se espera (octubre), tiene como decimos este peligro extra de dar confianza y poder al que niegua la posibilidad de un resurgimiento del virus pasada la primera pandemia. Es posible que esta negación, el recelo ante la eficacia del confinamiento, unida a la precaria situación política, económica y social; hagan aún más complejo retomar con eficiencia nuevos confinamientos estrictos en el futuro, por lo que la eficacia de las medidas que se tomen por ese entonces podrían bajar en eficiencia muchísimo respecto del actual confinamiento (y ya podemos ver en las gráficas las consecuencias de que dicha eficiencia baje por debajo del 50% cuando estemos en plena pandemia: líneas azul y roja).Nota importante: una vez más, si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (D) lo cual llevaría a dar marcha atrás inmediata. Pero existe el escenario más peligroso de todos los tenidos en cuenta, y es aquel en que el virus, dado que el factor estacional fuese importante, parezca desaparecer mucho más allá de octubre, momento en que se espera la segunda oleada; lo cual llevaría a que la desconfianza, la negación y los problemas económicos y políticos arrastrados imposibiliten tomar medidas de distanciamiento eficientes una segunda vez, llevando a la posibilidad de que la segunda oleada acabe arrasando con decenas de millones de nuevas víctimas y cientos de millones de afectados por todo el mundo.La sombra de lo que ocurrió en 1918 con la segunda oleada de la famosa gripe española (la que más personas mató con diferencia) parece revolotear sobre nuestras cabezas.Fijémonos en el escenario E).El escenario (E) supone que el confinamiento es indefinido, lo cual es irreal y empíricamente está ya descartado en estos momentos donde todos los países están ya proponiendo sus planes de desescalada; por lo que no lo tendré demasiado en cuenta (más detalles en el paper original). Simplemente comentar que, obviamente, si se mantiene el confinamiento estricto de manera indefinida, el virus acaba siendo controlado y no resurge.Resumen:- Los esfuerzos de distanciamiento social únicos pueden únicamente empujar el pico epidémico del SARS-CoV-2 hasta el otoño (o un poco más allá), lo que puede exacerbar aún más la carga de los recursos de cuidados intensivos si resulta que finalmente aumenta su transmisibilidad durante el invierno. El solapamiento con la gripe estacional es un problema añadido.- En ningún caso el distanciamiento social único puede erradicar el virus, siendo lo "mejor" que puede conseguirse eso que se denomina como inmunidad de grupo (o de "rebaño") al coste de innumerables vidas humanas. Además, se requerirían de pruebas serológicas masivas para comprender el alcance y la duración de dicha inmunidad natural (anticuerpos) al SARS-CoV-2, lo cual ayudará a determinar la dinámica pospandémica del virus. Es decir, que incluso una vez alcanzada la inmunidad de grupo, si la memoria de los anticuerpos generados no es permanente (algo que se puede asegurar casi con toda probabilidad), será necesario entonces comprender cuánto dura la inmunidad lograda a tan alto coste humano antes de que nuevas oleadas nos ataquen (lo cual se puede ver mejor en la dinámica que estudiamos en el artículo anterior).- Por lo tanto, el equipo del estudio formalmente reconoce que se necesitará sí o sí de una vigilancia sostenida y generalizada tanto a corto plazo, para implementar eficazmente medidas de distanciamiento social intermitentes, como a largo plazo, para evaluar la posibilidad de resurgimientos de la infección por SARS-CoV-2; algo que podría ocurrir tan tarde como en el año 2025, incluso después de un período prolongado de aparente eliminación.Próximas entradas.Para no hacer demasiado denso este artículo, dejaremos para una última entrada del blog el estudio del abordaje que el equipo de Harvard hace sobre la evolución (dinámica) del virus en el momento en que se toman medidas adicionales a la del confinamiento único. En concreto, la propuesta de realizar confinamientos intermitentes.
Si el factor ambiental es muy importanteEstas dos gráficas en concreto se basa en los siguientes valores para los parámetros: (D) poca inmunidad cruzada entre Betacoronavirus, poca variación estacional (primera figura), alta variación estacional (segunda figura), y veinte semanas de distanciamiento social efectivo (parte sombreada en lila en la imagen) antes de finalizar de manera más o menos abrupta el mismo.Los colores y formas de las líneas tienen el mismo significado que en el caso anterior.¿Qué significa pues este escenario D)?¡La interpretación es bastante interesante porque supone levantar el confinamiento alrededor de mediados/finales de julio, fecha aún más próxima que la del caso (C) a lo que los países se encuentran actualmente pensando hacer de manera gradual!:Vemos en la figura superior que, si hay poca inmunidad cruzada entre Betacoronavirus y el factor ambiental no es importante; si el confinamiento se levanta levantado 20 semanas después del 11 de marzo (mediados/finales de julio aproximadamente) ocurre lo siguiente según sea la eficiencia lograda durante esos dos meses de confinamiento:- Línea negra. 0% (ninguna intervención): Sin medidas de contención alguna, el caso es similar al del escenario (A). Picos de 20% de infectados y cientos de millones de muertos al cabo de pocos meses, momento en que se alcanza la inmunidad de grupo y la pandemia acaba.- Línea roja. Eficacia del confinamiento del 20%: en este caso se observa un aplanamiento todavía escaso de la curva (con y sin factor ambiental) lo cual supone que cualitativamente el resultado no sería demasiado diferente del caso anterior (no hacer nada). Esto no cuadra con los datos empíricos disponibles.- Línea azul. Eficacia del confinamiento del 40%: este caso es de nuevo interesante. Se aleja de la realidad en el caso de que el factor ambiental no sea importante (primera gráfica) pero se aproxima mucho más a la realidad que en el caso (C) cuando el factor ambiental sí es importante (segunda gráfica). En tal caso, el modelo sugiere que tras finalizar el confinamiento (suponiendo finales de julio como fecha límite) tendremos un repunte de casos gradual pero pronunciado que llevará a un pico (nueva oleada) a mediados de octubre.- Línea verde. Eficacia del confinamiento del 60%: este caso es todavía más interesante que en el escenario (C). En ambos casos (con y sin factor ambiental) los datos cuadran con la realidad empírica que observamos en estos momentos. Sin embargo, en el caso de que el factor ambiental no sea importante (primera gráfica), el repunte de casos será enorme (similar al del escenario C), llevando a la inmunidad de grupo para finales de año tras alcanzarse picos del 20% de infectados de media mundial (miles de millones de personas). ¡Recemos una última vez más porque este escenario tampoco sea el correcto!Si el factor estacional sí es importante, línea verde de la segunda gráfica del escenario (D), entonces el repunte de casos será muy gradual, ¡tan gradual y plano que es muy peligroso! Los contagios parecen desparecer y muchos pensarán que el virus está bajo control (incluso bien entrados ya en octubre, cosa que no sucedía en el caso C). Sin embargo; el factor estacional y la artificial eficacia del confinamiento (que dejará a la mayor parte de la población como susceptible de ser infectada), harían que para principios del año 2021 apareciera súbitamente una nueva oleada que, probablemente, pillaría por sorpresa (más que en el caso C) a gran parte de un mundo en pleno proceso de recuperación de la normalidad económica y social en ese momento. Además, y para más inri, esta nueva oleada se solaparía con la de la gripe estacional. Este escenario más probable del escenario (D) en realidad no es más que una copia del escenario (C) pero con la oleada atrasada un mes y medio. Sin embargo, este retraso podría confiar más aún a la población y a la clase política (necesitada de buenas notificas) pensando que el virus está erradicado, lo cual llevaría posiblemente a un negacionismo y a una relajación (que no detención) ante la búsqueda activa de tratamiento y/o vacunas.Esta segunda oleada "retrasada" (hasta enero del 2021) respecto de lo que se espera (octubre), tiene como decimos este peligro extra de dar confianza y poder al que niegua la posibilidad de un resurgimiento del virus pasada la primera pandemia. Es posible que esta negación, el recelo ante la eficacia del confinamiento, unida a la precaria situación política, económica y social; hagan aún más complejo retomar con eficiencia nuevos confinamientos estrictos en el futuro, por lo que la eficacia de las medidas que se tomen por ese entonces podrían bajar en eficiencia muchísimo respecto del actual confinamiento (y ya podemos ver en las gráficas las consecuencias de que dicha eficiencia baje por debajo del 50% cuando estemos en plena pandemia: líneas azul y roja).Nota importante: una vez más, si el factor ambiental resulta ser menos determinante de lo esperado por los expertos, estaríamos ante un repunte exponencial inmediato tras levantarse el confinamiento: línea verde del primer gráfico de este escenario (D) lo cual llevaría a dar marcha atrás inmediata. Pero existe el escenario más peligroso de todos los tenidos en cuenta, y es aquel en que el virus, dado que el factor estacional fuese importante, parezca desaparecer mucho más allá de octubre, momento en que se espera la segunda oleada; lo cual llevaría a que la desconfianza, la negación y los problemas económicos y políticos arrastrados imposibiliten tomar medidas de distanciamiento eficientes una segunda vez, llevando a la posibilidad de que la segunda oleada acabe arrasando con decenas de millones de nuevas víctimas y cientos de millones de afectados por todo el mundo.La sombra de lo que ocurrió en 1918 con la segunda oleada de la famosa gripe española (la que más personas mató con diferencia) parece revolotear sobre nuestras cabezas.Fijémonos en el escenario E).El escenario (E) supone que el confinamiento es indefinido, lo cual es irreal y empíricamente está ya descartado en estos momentos donde todos los países están ya proponiendo sus planes de desescalada; por lo que no lo tendré demasiado en cuenta (más detalles en el paper original). Simplemente comentar que, obviamente, si se mantiene el confinamiento estricto de manera indefinida, el virus acaba siendo controlado y no resurge.Resumen:- Los esfuerzos de distanciamiento social únicos pueden únicamente empujar el pico epidémico del SARS-CoV-2 hasta el otoño (o un poco más allá), lo que puede exacerbar aún más la carga de los recursos de cuidados intensivos si resulta que finalmente aumenta su transmisibilidad durante el invierno. El solapamiento con la gripe estacional es un problema añadido.- En ningún caso el distanciamiento social único puede erradicar el virus, siendo lo "mejor" que puede conseguirse eso que se denomina como inmunidad de grupo (o de "rebaño") al coste de innumerables vidas humanas. Además, se requerirían de pruebas serológicas masivas para comprender el alcance y la duración de dicha inmunidad natural (anticuerpos) al SARS-CoV-2, lo cual ayudará a determinar la dinámica pospandémica del virus. Es decir, que incluso una vez alcanzada la inmunidad de grupo, si la memoria de los anticuerpos generados no es permanente (algo que se puede asegurar casi con toda probabilidad), será necesario entonces comprender cuánto dura la inmunidad lograda a tan alto coste humano antes de que nuevas oleadas nos ataquen (lo cual se puede ver mejor en la dinámica que estudiamos en el artículo anterior).- Por lo tanto, el equipo del estudio formalmente reconoce que se necesitará sí o sí de una vigilancia sostenida y generalizada tanto a corto plazo, para implementar eficazmente medidas de distanciamiento social intermitentes, como a largo plazo, para evaluar la posibilidad de resurgimientos de la infección por SARS-CoV-2; algo que podría ocurrir tan tarde como en el año 2025, incluso después de un período prolongado de aparente eliminación.Próximas entradas.Para no hacer demasiado denso este artículo, dejaremos para una última entrada del blog el estudio del abordaje que el equipo de Harvard hace sobre la evolución (dinámica) del virus en el momento en que se toman medidas adicionales a la del confinamiento único. En concreto, la propuesta de realizar confinamientos intermitentes.
¿Cuánto tiempo tardará realmente la vacuna en llegar? [ENG]
nytimes.com[se estima que ]la vacuna podría llegar dentro de entre 12 y 18 meses. Sin embargo, la triste realidad detrás de este pronóstico optimista es que la vacuna probablemente no llegará tan pronto. Los ensayos clínicos casi nunca tienen éxito. Nunca antes hemos logrado una vacuna de coronavirus para humanos, y nuestro récord para desarrollar una vacuna completamente nueva es de al menos cuatro años, más tiempo del que el público o la economía pueden tolerar en referencia al distanciamiento social.[...Pero ]Así es como podríamos lograr lo imposible.
#3 Gracias por las puntualizaciones sobre el porcentaje de la inmunidad de grupo. Imagino que el porcentaje determinante dependerá del R0 del virus en cuestión, ¿cierto?
#16 Si, depende del R0. El R0 depende del virus, pero también de los contactos sociales que permitan infectar a otro. Estos contactos sociales dependen de muchas cosas. De la sociedas en si. Por ejemplo, puede ser que en España tengamos más contacto que en Alemania. De que un día haya sol y salga la gente a pasear o llueva y no lo haga.
La inmunidad de grupo para reducir la propagación tiene que ser tal que reduzca R0 por debajo de 1. Y solo hay dos maneras de crear esa inmunidad de grupo:
1) La inmunización (por vacuna o contagio que no mate al huesped)
2) El confinamiento.
Explicando el famoso paper: "Proyectando la dinámica de transmisión del SARS-CoV-2"
Hace ya unos días, la revista Science publicó uno de los papers más importantes de la historia reciente. Es un trabajo desarrollado por investigadores de Harvard y se titula: "Proyectando la dinámica de transmisión del SARS-CoV-2 durante el período pospandémico". Tenéis el original aquí, y una traducción al castellano que yo mismo realicé en este mismo blog aquí.El trabajo de estos autores de los departamentos de Inmunología y Enfermedades Infecciosas e Epidemiología de Harvard es a la vez simple y complejo de entender. Es complejo en cuanto a la metodología estadística y los modelos matemáticos utilizados (detalles al alcance de los más expertos en la materia que se recogen en un apartado de materiales complementarios que ya de por sí es casi un paper independiente por lo denso). Pero a la vez es simple en cuanto a lo "sencillo" que es entender los resultados de la aplicación de dichos modelos frente al mundo real.Voy a intentar ser breve en esta entrada para que todos entendamos los posibles escenarios que los expertos barajan en estos momentos para el periodo pandémico y el futuro pospandémico. Es decir, para la dinámica del virus: ¿qué es probable que ocurra con el SARS-CoV-2 en los próximos meses y años?Comentarios iniciales.Es necesario comentar antes de nada un par de cuestiones imprescindibles para poder entender mínimamente la dinámica del SARS-CoV-2:1) El COVID-19 es el nombre que se le ha dado a la enfermedad que causa el virus denominado SARS-CoV-2. Una cosa es la enfermedad (como por ejemplo, el SIDA), y otra el virus que lo causa (en el caso del SIDA es el VIH).2) El virus SARS-CoV-2 es un coronavirus (Orthocoronavirinae). Para la subfamilia del coronavirus existen a su vez cuatro géneros: Alphacoronavirus, Betacoronavirus, Gammacoronavirus y Deltacoronavirus. El SARS-CoV-2 pertenece al género Betacoronavirus.3) Además del SARS-CoV-2, existen muchos otros virus de la subfamilia coronavirus que son capaces de transmitirse de humano a humano. Entre ellos tenemos al MERS-CoV (que produce desde el 2015 la enfermedad aún en activo llamada: síndrome respiratorio de Oriente Medio), el SARS-CoV-1 (que apareció y desapareció entre los años 2002/2003 produciendo la enfermedad: síndrome respiratorio agudo grave), y otros muchos virus que por su levedad cuadran y se aglutinan en lo que se llama resfriado común. Es decir, que eso que nos contagia casi cada año y que denominamos resfriado (enfermedad), es en realidad producto casi siempre de un tipo de los restantes coronavirus capaces de infectar humanos.4) El 15% de los resfriados son causados por coronavirus, y de estos casos, la mayor parte los producen los coronavirus: HCoV-229E, HCoV-NL63, HCoV-0C43 y HCoV-HKU1.5) De entre estos cuatro, sólo dos pertenecen al mismo género Betacoronavirus del SARS-CoV-1, SARS-CoV-2, y el MERS-CoV. Se trata del HCoV-OC43 y el HCoV-HKU1.6) Todos los Betacoronavirus presentan, dada su similitud filogenética, cierta inmunidad cruzada. Se conoce la realidad este proceso gracias al estudio de los coronavirus del resfriado común. Por ejemplo; pasar el HCoV-OC43 te inmuniza hasta cierto punto y tiempo frente al HCoV-HKU1, y viceversa. En el estudio del que estamos hablando se supone, según el escenario, que también existe cierta inmunidad cruzada entre estos virus "del resfriado" y el SARS-CoV-2. Y modelan la dinámica del COVID19 otorgando varios valores a dicho factor de inmunidad cruzada (de más débil a más fuerte).7) Por otra parte, el estudio también basa los escenarios pronosticados a partir de lo que denominan factor estacional. Es decir, cuánto y cómo afecta al virus los climas húmedos y las temperaturas más altas. En este sentido, varían también en las simulaciones que realizan los números para este factor.8) También utilizan, por supuesto, el factor más importante para todo modelo epidemiológico: la inmunidad de grupo. Es decir, cuándo y cómo se alcanzará el punto en que más del 60% de la población deja de ser susceptible al virus (por haber pasado la enfermedad). En este sentido, cobra especial importancia para entender la dinámica futura conocer cuánta inmunidad (anticuerpos) produce nuestro cuerpo tras pasar la infección, y qué "memoria" o duración tienen dichos anticuerpos. En este sentido, y a raíz de lo que se sabe de los virus del resfriado HCoV-OC43 y HCoV-HKU1, proponen que la inmunidad dura entre 40 semanas (en el peor escenario) y 104 semanas (en el mejor caso). La inmunidad permanente la tienen en cuenta, pero se sabe que es un escenario MUY poco probable.9) Finalmente, toman como parámetro para la simulación la intensidad y el momento de las medidas de control que tomen los gobiernos (aunque este punto lo retomaremos en futuras entradas del blog).Simulando la transmisión de SARS-CoV-2.En el paper el equipo de investigación explica que han utilizado el modelo epidemiológico de transmisión SEIRS y que lo han ajustado a partir de todos los datos disponibles para los Betacoronavirus HCoV-OC43 y HCoV-HKU1 que, como hemos dicho, son muy cercanos filogenéticamente al SARS-CoV-2. Para justificar el buen ajuste de este modelo muestran las primeras dos figuras (Fig.1 y Fig.2) que no nos interesan demasiado para lo que trataremos aquí. Demos por bueno el modelo y veamos que nos dice:La primera gráfica de interés es la que denominan Fig. 3 "Distintos escenarios de prevalencia para el SARS-CoV-2 en regiones templadas durante los próximos cinco años". Se trata de la siguiente figura: Los picos rojos y azules son para los Betacoronavirus del resfriado común, mientras que los picos en negros son los del SARS-CoV-2. En el eje X tenemos los años por venir (se ve una línea vertical en negro indicando donde estamos ahora: abril del 2020). En el eje Y tenemos grosso modo la cantidad de infectados por cada 1000 habitantes: por ponerlo en claro, cuánto más alto el pico más cantidad de infectados en general. Si el pico llega cerca del 100, eso indicaría que una gran parte de toda la población mundial estaría infectada en ese momento.Fijémonos en el escenario A).
Los picos rojos y azules son para los Betacoronavirus del resfriado común, mientras que los picos en negros son los del SARS-CoV-2. En el eje X tenemos los años por venir (se ve una línea vertical en negro indicando donde estamos ahora: abril del 2020). En el eje Y tenemos grosso modo la cantidad de infectados por cada 1000 habitantes: por ponerlo en claro, cuánto más alto el pico más cantidad de infectados en general. Si el pico llega cerca del 100, eso indicaría que una gran parte de toda la población mundial estaría infectada en ese momento.Fijémonos en el escenario A). Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (A) χ 3X = 0.3, χ X3 = 0, 1 / σ 3 = 40 semanas, f = 0.2.- χ 3X = 0.3, χ X3 = 0, indica que en este escenario hay muy poca inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado no implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 40, implica una corta duración (40 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados no nos otorgan mucha protección conforme pasan los meses. Obviamente no se estima inmunidad permanente para este escenario.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario A)?Que si la inmunidad cruzada con los coronavirus del resfriado común es baja, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad no dura más de 40 semanas, y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos un gran pico en la primera pandemia (en la que estamos) y recurrentes brotes anuales que afectarían a una parte muy importante de la población: ¡algo así como 1 de cada 5 personas pasarían el COVID19 cada año!Fijémonos en el escenario B).
Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (A) χ 3X = 0.3, χ X3 = 0, 1 / σ 3 = 40 semanas, f = 0.2.- χ 3X = 0.3, χ X3 = 0, indica que en este escenario hay muy poca inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado no implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 40, implica una corta duración (40 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados no nos otorgan mucha protección conforme pasan los meses. Obviamente no se estima inmunidad permanente para este escenario.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario A)?Que si la inmunidad cruzada con los coronavirus del resfriado común es baja, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad no dura más de 40 semanas, y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos un gran pico en la primera pandemia (en la que estamos) y recurrentes brotes anuales que afectarían a una parte muy importante de la población: ¡algo así como 1 de cada 5 personas pasarían el COVID19 cada año!Fijémonos en el escenario B). Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (B) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = 104 semanas, f = 0.2.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco se trata de inmunidad permanente.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario B)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos un gran pico en la primera pandemia (en la que estamos) y luego recurrentes brotes cada dos años que afectarían a una parte relativamente importante de la población: ¡algo así como 1 de cada 6 personas pasarían el COVID19 cada dos años! Entre estos dos años de brotes relativamente importantes habrían pequeños brotes en los años intermedios.Nota: Es interesante ver en esta gráfica cómo suponer una alta inmunidad cruzada hace que los casos de resfriado común también descenderían a nivel mundial debido al COVID19.Fijémonos en el escenario C).
Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (B) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = 104 semanas, f = 0.2.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco se trata de inmunidad permanente.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario B)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos un gran pico en la primera pandemia (en la que estamos) y luego recurrentes brotes cada dos años que afectarían a una parte relativamente importante de la población: ¡algo así como 1 de cada 6 personas pasarían el COVID19 cada dos años! Entre estos dos años de brotes relativamente importantes habrían pequeños brotes en los años intermedios.Nota: Es interesante ver en esta gráfica cómo suponer una alta inmunidad cruzada hace que los casos de resfriado común también descenderían a nivel mundial debido al COVID19.Fijémonos en el escenario C). Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (C) χ 3X = 0.7, χ X3 = 0, 1 / σ 3= 104 semanas, f = 0.4.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco se trata de inmunidad permanente.- f = 0.4, implica alta variación estacional. En este caso, el SARS-CoV-2 se vería bastante afectado por los cambios ambientales de humedad y temperatura. Esta es la única variable que se modifica con respecto al escenario B).¿Qué significa pues este escenario C)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es bastante importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos como se reduciría el tamaño máximo de la onda de infección inicial, pero que se llegarían a producir brotes en invierno mucho más severos a partir de ese momento [compárese con (B)].Nota: ¡Se puede observar que, contrariamente a lo que muchos creen, el hecho de que el factor ambiental sea importante podría llevar a escenarios mucho más severos que en el caso donde los cambios estacionales no son relevantes!Fijémonos en el escenario D).
Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (C) χ 3X = 0.7, χ X3 = 0, 1 / σ 3= 104 semanas, f = 0.4.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco se trata de inmunidad permanente.- f = 0.4, implica alta variación estacional. En este caso, el SARS-CoV-2 se vería bastante afectado por los cambios ambientales de humedad y temperatura. Esta es la única variable que se modifica con respecto al escenario B).¿Qué significa pues este escenario C)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es bastante importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos como se reduciría el tamaño máximo de la onda de infección inicial, pero que se llegarían a producir brotes en invierno mucho más severos a partir de ese momento [compárese con (B)].Nota: ¡Se puede observar que, contrariamente a lo que muchos creen, el hecho de que el factor ambiental sea importante podría llevar a escenarios mucho más severos que en el caso donde los cambios estacionales no son relevantes!Fijémonos en el escenario D). Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (D) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = infinito, f = 0.2.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = infinito, implica que la inmunidad es permanente. Una vez pasas el COVID19 los anticuerpos de tu cuerpo impiden que jamás vuelvas a pasar la enfermedad.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario D)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es permanente (infinita en el tiempo), y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos que la inmunidad de grupo podría eliminar por completo al virus para siempre tras la infección inicial en la que estamos.Nota: si este, poco probable, escenario fuese el bueno, es interesante notar como de camino acabaríamos con las dos cepas de Betacoronavirus que nos causan resfriado común (líneas rojas y azul). ¡El HCoV-OC43 y el HCoV-HKU1 también serían erradicados!Fijémonos en el escenario E).
Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (D) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = infinito, f = 0.2.- χ 3X = 0.7, χ X3 = 0, indica que en este escenario hay bastante inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado sí implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = infinito, implica que la inmunidad es permanente. Una vez pasas el COVID19 los anticuerpos de tu cuerpo impiden que jamás vuelvas a pasar la enfermedad.- f = 0.2, implica poca variación estacional. En este caso, el SARS-CoV-2 se vería relativamente poco afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario D)?Que si la inmunidad cruzada con los coronavirus del resfriado común es alta, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es permanente (infinita en el tiempo), y el factor ambiental (estacional) es poco importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos que la inmunidad de grupo podría eliminar por completo al virus para siempre tras la infección inicial en la que estamos.Nota: si este, poco probable, escenario fuese el bueno, es interesante notar como de camino acabaríamos con las dos cepas de Betacoronavirus que nos causan resfriado común (líneas rojas y azul). ¡El HCoV-OC43 y el HCoV-HKU1 también serían erradicados!Fijémonos en el escenario E). Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (E) χ 3X = 0.3, χ X3 = 0.3, 1 / σ 3 = 104 semanas, f = 0.4.- χ 3X = 0.3, χ X3 = 0, indica que en este escenario hay muy poca inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado no implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco es permanente.- f = 0.4, implica alta variación estacional. En este caso, el SARS-CoV-2 se vería bastante afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario E)?Que si la inmunidad cruzada con los coronavirus del resfriado común es baja, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es bastante importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos que un resurgimiento del SARS-CoV-2 podría ocurrir tan tarde como en el 2024 después de un período de eliminación aparente.Nota: es interesante notar como el hecho de que la inmunidad no sea permanente lleva a que incluso en las situaciones más desfavorables para el virus, éste pueda resurgir tras varios picos y un periodo de varios años donde falsamente parece que se logró erradicar el virus, no siendo el caso ya que una vez la inmunidad de 104 semanas deja de tener efecto el virus reaparece con fuerza.Resumen:- Si la inmunidad al SARS-CoV-2 no es permanente, es muy probable que entre en circulación regular.- La alta variación estacional en la transmisión conduce a una menor incidencia máxima durante la onda pandémica inicial, pero a brotes recurrentes más severos en los sucesivos inviernos.- Si la inmunidad al SARS-CoV-2 es permanente, el virus podría desaparecer tras cinco años o más después de causar el actual brote.- Unos bajos niveles de inmunidad cruzada frente a los otros Betacoronavirus (y sin inmunidad permanente) podrían hacer que el SARS-CoV-2 parezca extinguirse, solo para resurgir después de unos años.- El SARS-CoV-2 puede proliferar en cualquier época del año. En todos los escenarios modelados el SARS-CoV-2 fue capaz de producir un brote sustancial, independientemente del tiempo de establecimiento. Los establecimientos de invierno/primavera favorecieron los brotes con picos más bajos, mientras que los establecimientos de otoño/invierno condujeron a brotes más severos. Y cuanta más dependencia estacional exista, más severo y agudo será el brote anual (o bienal).Próximas entradas.Para no hacer demasiado denso este artículo, dejaremos para próximas entradas del blog el estudio del abordaje que el equipo de Harvard hace sobre la evolución (dinámica) del virus en el momento en que se toman medidas activas frente a la pandemia. Es decir, qué posibles escenarios nos esperan para el virus según sea la actitud tomada a partir de ahora por los gobiernos y la ciencia en general frente al COVID19.
Esta gráfica en concreto se basa en los siguientes valores para los parámetros más importantes del modelo: (E) χ 3X = 0.3, χ X3 = 0.3, 1 / σ 3 = 104 semanas, f = 0.4.- χ 3X = 0.3, χ X3 = 0, indica que en este escenario hay muy poca inmunidad cruzada entre los Betacoronavirus del resfriado común y el SARS-CoV-2. Es decir, que pillar un resfriado no implicaría tener mucha menos probabilidad de pillar COVID19.- 1 / σ 3 = 104, implica una "larga" duración (104 semanas) de inmunidad contra el SARS-CoV-2 una vez pasada la enfermedad: es decir, los anticuerpos generados nos otorgan bastante protección conforme pasan los meses. Pero tampoco es permanente.- f = 0.4, implica alta variación estacional. En este caso, el SARS-CoV-2 se vería bastante afectado por los cambios ambientales de humedad y temperatura.¿Qué significa pues este escenario E)?Que si la inmunidad cruzada con los coronavirus del resfriado común es baja, la inmunidad que nuestro cuerpo adquiere tras pasar la enfermedad es duradera (alrededor de 104 semanas), y el factor ambiental (estacional) es bastante importante; en caso de no poseerse vacunas, tratamientos, ni tomarse medidas de contención, en la dinámica del virus veríamos que un resurgimiento del SARS-CoV-2 podría ocurrir tan tarde como en el 2024 después de un período de eliminación aparente.Nota: es interesante notar como el hecho de que la inmunidad no sea permanente lleva a que incluso en las situaciones más desfavorables para el virus, éste pueda resurgir tras varios picos y un periodo de varios años donde falsamente parece que se logró erradicar el virus, no siendo el caso ya que una vez la inmunidad de 104 semanas deja de tener efecto el virus reaparece con fuerza.Resumen:- Si la inmunidad al SARS-CoV-2 no es permanente, es muy probable que entre en circulación regular.- La alta variación estacional en la transmisión conduce a una menor incidencia máxima durante la onda pandémica inicial, pero a brotes recurrentes más severos en los sucesivos inviernos.- Si la inmunidad al SARS-CoV-2 es permanente, el virus podría desaparecer tras cinco años o más después de causar el actual brote.- Unos bajos niveles de inmunidad cruzada frente a los otros Betacoronavirus (y sin inmunidad permanente) podrían hacer que el SARS-CoV-2 parezca extinguirse, solo para resurgir después de unos años.- El SARS-CoV-2 puede proliferar en cualquier época del año. En todos los escenarios modelados el SARS-CoV-2 fue capaz de producir un brote sustancial, independientemente del tiempo de establecimiento. Los establecimientos de invierno/primavera favorecieron los brotes con picos más bajos, mientras que los establecimientos de otoño/invierno condujeron a brotes más severos. Y cuanta más dependencia estacional exista, más severo y agudo será el brote anual (o bienal).Próximas entradas.Para no hacer demasiado denso este artículo, dejaremos para próximas entradas del blog el estudio del abordaje que el equipo de Harvard hace sobre la evolución (dinámica) del virus en el momento en que se toman medidas activas frente a la pandemia. Es decir, qué posibles escenarios nos esperan para el virus según sea la actitud tomada a partir de ahora por los gobiernos y la ciencia en general frente al COVID19.
Oficina Presupuestos Congreso EEUU ve contracción PIB de 12% en segundo trimestre
es.investing.comWASHINGTON, 24 abr (Reuters) - La economía de Estados Unidos enfrenta un futuro inmediato sombrío, con un PIB que probablemente se contraerá un 12% en el segundo trimestre y el déficit federal crecerá a 3,7 billones de dólares, según proyecciones publicadas el viernes por Oficina de Presupuesto del Congreso. La tasa de desempleo probablemente alcanzará un 16% en el tercer trimestre, según las estimaciones de la oficina no partidista.
Hasta ahora Angela Merkel ha acertado mucho en sus predicciones. Veremos con ésta: "Los hospitales se preparan para un nuevo aumento de infecciones que podría ser provocado por el fin del confinamiento."
Y lo que más me preocupa es que aquí, con el tema de pasear a los chavales, estamos haciendo de facto una gran relajación en nuestro confinamiento particular. Yo también temo que a partir de la semana que viene el número de casos repuntará aquí también en España con bastante probabilidad.
#51 Aquí no hemos hecho nada. Encerrar a la gente para que no proteste y mantener a todos los ancianos juntos en las residencias. Eso sí, en propaganda hemos sido los primeros. Medidas políticas, todas pensando en las elecciones y la opinión pública. La foto, el lema, la guerra, la lucha... Mucho pasteleo y nada más.
Si alguien piensa que se puede mantener un confinamiento por un tiempo indefinido tienen un problema, que es olvidarse de que en un punto las bajas relacionadas con el confinamiento serán mayores a las de la epidemia.
Varias cosas a tener en cuenta sobre éste asunto:
1) La crisis económica postpandemia va a ser devastadora y puede que mate más gente de hambre (en según qué países) que el propio virus.
2) La inmunidad de grupo contendrá en los próximos meses (en cuanto abran un poco las puertas del confinamiento los picos irán hacia arriba en todas partes) la ACTUAL pandemia. Pero la inmunidad en los betacoronavirus (del que el SARS-CoV-2 es un miembro más, hermano de varios otros que causan el resfriado común); se sabe que NO es de larga duración, y que nuestro sistema inmune pierde eficacia frente al virus pasados alrededor de 40 semanas (simplemente los anticuerpos generados por nuestro cuerpo pierden eficiencia conforme pasan los meses).
3) Esta pérdida de inmunidad significa que no sólo es cierto que el 70% (o más) pillaremos en la actual pandemia el COVID-19, sino que dentro de varios meses, la población habrá perdido esta inmunidad de grupo, lo cual abrirá la puerta a una nueva oleada de la enfermedad: posiblemente también en forma de pandemia. Hay un paper de Harvard publicado en la revista Science donde se explica todo muy claro, con todo lujo de detalles.
4) En resumen: si la vacuna o antivirales (deben ser varios en forma de cóctel como en el caso de VIH) no llegan, como es probable, hasta dentro de 24 meses, hay tiempo para que suframos al menos tres oleadas más una vez esta se relaje un poco debido a la inmunidad TEMPORAL de grupo.
5) El día que llegue la vacuna, será del estilo de la gripe: habrá que inyectarse cada año una para adquirir nueva inmunidad (ya que los anticuerpos inducidos por la primera vacuna también van a decaer en eficiencia con el tiempo).
#1 Me has un alegría porque después del tute que me he pegado, parece que eres el único que lo ha leído ![]() . Yo pensé que todos iban a ver la importancia que tiene lo que dicen en el ensayo pero no sé, o la gente en general no lo han entendido, o pasan ya del asunto; o han visto un texto muy largo y ni lo han mirado. En fin. Gracias!
. Yo pensé que todos iban a ver la importancia que tiene lo que dicen en el ensayo pero no sé, o la gente en general no lo han entendido, o pasan ya del asunto; o han visto un texto muy largo y ni lo han mirado. En fin. Gracias!
#2 de nada con ver las conclusiones es suficiente, y dan para pensar en que hacer a partir de un mes. Ya se ve como China empieza otra ola, sería un buen momento para pensar escenarios de acción. A nivel personal es facil, cuidar de nuestros mayores y de nosotros todo lo posible. A nivel de empresa no lo tengo muy claro, pensare que opciones hay y lo plantearé la semana que viene. Gracias de nuevo
Proyectando la dinámica de transmisión del SARS-CoV-2 durante el período pospandémico (traducción)
Os dejo la traducción de un interesante paper publicado por la revista Science hace pocos días. La mayor parte de los investigadores involucrados pertenecen a la Universidad de Harvard. Espero os resulte de interés. La traducción completa no cabe en un artículo de Menéame pero podéis ver el resto aquí.=================================================================================Proyectando la dinámica de transmisión del SARS-CoV-2 durante el período pospandémicoStephen M. Kissler 1 , * , Christine Tedijanto2 , * , Edward Goldstein 2 , Yonatan H. Grad 1 , † , ‡ , Marc Lipsitch 2 , † , ‡1 Departamento de Inmunología y Enfermedades Infecciosas, Harvard TH Chan School of Public Health, Boston, MA, EE. UU.2 Departamento de Epidemiología, Harvard TH Chan School of Public Health, Boston, MA, EE. UU.‡ Autor correspondiente. Correo electrónico: mlipsitc@hsph.harvard.edu (ML); ygrad@hsph.harvard.edu (YHG)* Estos autores contribuyeron igualmente a este trabajo y son coautores principales.Science 14 de abril de 2020:AbstractEs urgente entender el futuro de la transmisión del síndrome respiratorio agudo severo - coronavirus 2 (SARS-CoV-2). Utilizamos estimaciones de estacionalidad, inmunidad e inmunidad cruzada para los betacoronavirus OC43 y HKU1 a partir de datos de series temporales de los EE.UU. para formar un modelo de transmisión de SARS-CoV-2. Proyectamos que los brotes recurrentes de SARS-CoV-2 durante el invierno probablemente ocurrirán después de la actual onda pandémica inicial más grave. En ausencia de otras intervenciones, una métrica clave para el éxito del distanciamiento social es si se exceden las capacidades de atención médica crítica. Para evitar esto, el distanciamiento social prolongado o intermitente puede ser necesario en 2022. Las intervenciones adicionales, incluida la capacidad de atención médica crítica ampliada y una terapia efectiva, mejorarían el éxito del distanciamiento intermitente y acelerarían la adquisición de la inmunidad colectiva. Se necesitan con urgencia estudios serológicos longitudinales para determinar el alcance y la duración de la inmunidad al SARS-CoV-2. Incluso en el caso de una eliminación aparente, la vigilancia del SARS-CoV-2 debe mantenerse ya que un resurgimiento del contagio podría ser posible hasta el 2024.La actual pandemia de síndrome respiratorio agudo-coronavirus 2 (SARS-CoV-2) ha causado casi 500,000 casos detectados de la enfermedad por coronavirus 2019 (COVID-19) y se cobró más de 20,000 vidas en todo el mundo a partir del 26 de marzo de 2020 ( 1 ). La experiencia de China, Italia y los Estados Unidos demuestra que COVID-19 puede abrumar incluso las capacidades de atención médica de naciones con buenos recursos ( 2 - 4). Sin tratamientos farmacéuticos disponibles, las intervenciones se han centrado en el rastreo de contactos, la cuarentena y el distanciamiento social. La intensidad requerida, la duración y la urgencia de estas respuestas dependerán tanto de cómo se desarrolle la onda pandémica inicial como de la dinámica de transmisión posterior del SARS-CoV-2. Durante la ola pandémica inicial, muchos países han adoptado medidas de distanciamiento social y algunos, como China, las están levantando gradualmente después de lograr un control adecuado de la transmisión. Sin embargo, para mitigar la posibilidad de resurgimiento de la infección, pueden requerirse períodos prolongados o intermitentes de distanciamiento social. Después de la ola pandémica inicial, el SARS-CoV-2 podría seguir a su pariente genético más cercano, el SARS-CoV-1, y ser erradicado por medidas intensivas de salud pública después de causar una epidemia breve pero intensa (5 ), pero cada vez más, las autoridades de salud pública consideran que este escenario es poco probable ( 6 ). Alternativamente, la transmisión del SARS-CoV-2 podría parecerse a la de la gripe pandémica al circular estacionalmente después de causar una ola global de infección inicial ( 7 ). Tal escenario podría reflejar la aparición previa de coronavirus humanos conocidos de origen zoonótico, por ejemplo, el coronavirus humano (HCoV) OC43 ( 8 ). Distinguir entre estos escenarios es clave para formular una respuesta de salud pública efectiva y sostenida al SARS-CoV-2.La dinámica de transmisión pandémica y postpandémica del SARS-CoV-2 dependerá de factores que incluyen el grado de variación estacional en la transmisión, la duración de la inmunidad y el grado de inmunidad cruzada entre el SARS-CoV-2 y otros coronavirus, así como la intensidad y el momento de las medidas de control. El SARS-CoV-2 pertenece al género betacoronavirus, que incluye el coronavirus SARS-CoV-1, el coronavirus MERS y otros dos coronavirus humanos, HCoV-OC43 y HCoV-HKU1. Los coronavirus SARS-CoV-1 y MERS causan enfermedades graves con tasas de letalidad aproximadas de 9 y 36% respectivamente, pero la transmisión de ambos se ha mantenido limitada ( 9). Las infecciones por HCoV-OC43 y HCoV-HKU1 pueden ser asintomáticas o estar asociadas con enfermedades leves a moderadas del tracto respiratorio superior. Estos HCoV se consideran la segunda causa más común del resfriado común ( 9 ). HCoV-OC43 y HCoV-HKU1 causan brotes anuales de enfermedades respiratorias durante el invierno en regiones templadas ( 10 , 11 ), lo que sugiere que el clima de invierno y los comportamientos del huésped pueden facilitar la transmisión, como es el caso de la gripe ( 12 - 14 ). La inmunidad a HCoV-OC43 y HCoV-HKU1 parece disminuir considerablemente dentro de un año ( 15 ), mientras que la infección por SARS-CoV-1 puede inducir una inmunidad más duradera ( 16 ). Los betacoronavirus pueden inducir respuestas inmunes entre sí: la infección por SARS-CoV-1 puede generar anticuerpos neutralizantes contra HCoV-OC43 ( 16 ) y la infección por HCoV-OC43 puede generar anticuerpos de reacción cruzada contra SARS-CoV-1 ( 17 ). Si bien las investigaciones sobre el espectro de enfermedades causadas por el SARS-CoV-2 están en curso, la evidencia reciente indica que la mayoría de los casos experimentan una enfermedad leve a moderada con una ocurrencia más limitada de infección grave de las vías respiratorias inferiores ( 18 ). Se estima que las tasas actuales de letalidad de casos de COVID-19 oscilan entre 0.6% y 3.5% ( 19 , 20), lo que sugiere una gravedad menor que el SARS-CoV-1 y el MERS, pero una gravedad mayor que HCoV-OC43 y HCoV-HKU1. La alta infecciosidad cerca del comienzo de los síntomas, a menudo leves, hace que el SARS-CoV-2 sea mucho más difícil de controlar con intervenciones basadas en casos confirmados como pruebas intensivas, aislamiento y rastreo, en comparación con los coronavirus SARS-CoV-1 y MERS ( 21 ).Las pruebas intensivas y las intervenciones basadas en casos confirmados hasta ahora han formado la pieza central de los esfuerzos de control en algunos lugares, como Singapur y Hong Kong ( 22 ). Muchos otros países están adoptando medidas denominadas "distanciamiento social" o "distanciamiento físico", cerrando escuelas y lugares de trabajo y limitando el tamaño de las reuniones. El objetivo de estas estrategias es reducir la intensidad máxima de la epidemia ("aplanar la curva") ( 22 ), reducir el riesgo de abrumar los sistemas de salud y ganar tiempo para desarrollar tratamientos y vacunas. Para que el distanciamiento social haya podido revertir la epidemia en China, el número de reproducción efectiva debe haber disminuido en al menos un 50-60%, suponiendo una línea de base R 0 de entre 2 y 2.5 ( 22). Mediante medidas de control intensivo, Shenzhen pudo reducir el número de reproducción efectiva en un 85% (estimado) ( 23 ). Sin embargo, no está claro como de bien estos descensos en R 0 pueden generalizarse a otros entornos: los datos recientes de Seattle sugieren que el número de reproducción básica solo ha disminuido a aproximadamente 1.4, o en aproximadamente 30-45% suponiendo un R 0 de referencia entre 2 y 2,5 ( 24 ). Además, es posible que las medidas de distanciamiento social deban durar meses para controlar efectivamente la transmisión y mitigar la posibilidad de resurgimiento ( 25 ).Una medida clave para el éxito de las intervenciones de distanciamiento social es si se exceden las capacidades de atención médica crítica. Los estudios de modelado ( 26 ) y la experiencia del brote de Wuhan ( 2 ) indican que las capacidades de atención médica crítica, incluso en países de altos ingresos, pueden superarse ampliamente si las medidas de distanciamiento no se implementan de manera rápida o lo suficientemente contundente. Para aliviar estos problemas, los enfoques para aumentar la capacidad de atención crítica han incluido la construcción rápida o la reutilización de instalaciones hospitalarias y la consideración de una mayor fabricación y distribución de ventiladores ( 27 - 30 ). Los tratamientos que reducen la proporción de infecciones que conducen a enfermedades graves podrían tener un efecto similar al reducir la carga sobre los sistemas de salud.Este estudio identifica y utiliza factores virales, ambientales e inmunológicos que en combinación determinarán la dinámica del SARS-CoV-2. Integramos nuestros hallazgos en un modelo matemático para proyectar escenarios potenciales para la transmisión del SARS-CoV-2 a través de los períodos de pandemia y pospandémica e identificamos los datos clave que aún se necesitan para determinar qué escenarios es probable que se desarrollen. Luego, utilizando el modelo, evaluamos la duración e intensidad de las medidas de distanciamiento social que podrían ser necesarias para mantener el control del SARS-CoV-2 en los próximos meses bajo las capacidades de cuidados críticos médicos existentes.Dinámica de transmisión de HCoV-OC43 y HCoV-HKU1Utilizamos datos de los Estados Unidos para modelar la transmisión de betacoronavirus en regiones templadas y para proyectar la posible dinámica de la infección por SARS-CoV-2 hasta el año 2025. Primero evaluamos el papel de la variación estacional, la duración de la inmunidad y la inmunidad cruzada en el transmisibilidad de HCoV-OC43 y HCoV-HKU1 en los EE.UU. Utilizamos el porcentaje semanal de pruebas de laboratorio positivas para HCoV-OC43 y HCoV-HKU1 ( 31 ) multiplicado por la proporción ponderada semanal de visitas al médico debido a una enfermedad similar a la influenza (gripe) (ILI) ( 32 , 33), para aproximar la incidencia histórica de betacoronavirus en los EE.UU. dentro de una escala constante. Este indicador es proporcional a la incidencia bajo un conjunto de supuestos descritos en los materiales y métodos complementarios. Para cuantificar la variación en la fuerza de transmisión a lo largo del tiempo, estimamos el número de reproducción efectiva semanal, definido como el número promedio de infecciones secundarias causadas por un solo individuo infectado ( 34 , 35). Los números de reproducción efectivos para cada uno de los betacoronavirus mostraron un patrón estacional, con picos anuales en el número de reproducción efectiva ligeramente anterior a los de las curvas de incidencia (fig. S1). Limitamos nuestro análisis de estimaciones "estacionales" basadas en muestras adecuadas, definidas como la de la semana 40 a la semana 20 del año siguiente; aproximadamente de octubre a mayo. Tanto para el HCoV-OC43 como para el HCoV-HKU1, el número de reproducción efectiva generalmente alcanzó su punto máximo entre octubre y noviembre y su decaimiento entre febrero y mayo. Durante las cinco temporadas incluidas en nuestros datos (2014-2019), el número medio de reproducción efectiva máxima fue 1.85 (rango: 1.61-2.21) para HCoV-HKU1 y 1.56 (rango: 1.54-1.80) para HCoV-OC43 después de eliminar los valores atípicos (cinco para HCoV-HKU1, cero para HCoV-OC43).Para cuantificar la contribución relativa de la inmunidad frente al forzamiento estacional en la dinámica de transmisión de los betacoronavirus, adaptamos un modelo de regresión ( 36 ) que expresaba el número de reproducción efectivo para cada cepa (HKU1 y OC43) como el producto de una constante de transmisibilidad de referencia (relacionada al número de reproducción básico R0 y la proporción de la población susceptible al comienzo de cada temporada), el decaimiento de la población susceptible debido a la infección con la misma cepa, el decaimiento debido a la infección con la otra cepa y añadimos una horquilla para capturar una variación (forzamiento estacional). Estas covariables pudieron explicar la mayor parte de la variabilidad observada en los números de reproducción efectivos (R2 ajustado : 74,3%). Los efectos multiplicativos estimados de cada una de estas covariables en el número de reproducción semanal se representan en la figura 1. Como se esperaba, la reducción de la población susceptible para cada cepa se correlacionó negativamente con la transmisibilidad de esa cepa. La reducción de personas susceptibles para cada cepa también se correlacionó negativamente con el número de reproducción de la otra cepa de betacoronavirus, lo que proporciona evidencia de inmunidad cruzada. Por unidad de incidencia, el efecto de la inmunización cruzada siempre fue menor que el efecto de la inmunidad a la propia cepa (tabla S1), pero el impacto general de la inmunidad cruzada en el número de reproducción podría ser sustancial si una de las cepas de inmunización cruzada tuvo un gran brote (p. ej., HCoV-OC43 en 2014-15 y 2016-17). La proporción de inmunización cruzada frente a los efectos de autoinmunización fue mayor para HCoV-HKU1 que para HCoV-OC43, lo que sugiere que HCoV-OC43 confiere una inmunidad cruzada más fuerte. La estacionalidad parece impulsar el aumento de la transmisibilidad al comienzo de la temporada (finales de octubre hasta principios de diciembre), mientras que el decaimiento de los susceptibles desempeña un papel relativamente mayor en la disminución de la transmisibilidad hacia el final de la temporada. Los coeficientes del factor de estacionalidad fue bastante consistente en todas las estaciones para cada variedad y carecieron de una clara correlación con la incidencia en temporadas anteriores, lo cual es consistente con resultados experimentales que demuestran una disminución sustancial de la inmunidad frente a estos virus al cabo de un año (15 ).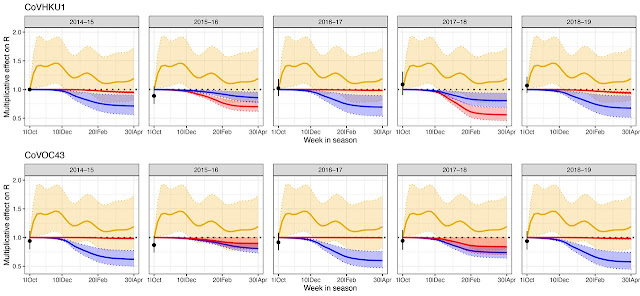 Fig. 1 Efectos de la reducción de la población susceptible y la estacionalidad sobre el número efectivo de reproducción por cepa y temporada.Efectos multiplicativos estimados de la incidencia de HCoV-HKU1 (rojo), incidencia de HCoV-OC43 (azul) y factor estacional (oro) sobre los números de reproducción efectiva semanal de HCoV-HKU1 (paneles superiores) y HCoV-OC43 (abajo), con intervalos de confianza del 95%. El punto negro (con un intervalo de confianza del 95%) trazado al comienzo de cada temporada es el coeficiente estimado para esa cepa y temporada en comparación con la temporada 2014-15 HCoV-HKU1. La horquilla del factor estacional se establece en 1 en la primera semana de la temporada (sin impedimentos). En el eje x, la primera "semana en la temporada" corresponde a la semana epidemiológica 40.Integramos estos hallazgos en un modelo compartimental de dos cepas usando las ecuaciones diferenciales ordinarias (EDO) del modelo epidemilógico: susceptible-expuesto-infeccioso-recuperado-susceptible (SEIRS) para describir la dinámica de transmisión de HCoV-OC43 y HCoV-HKU1 (fig. S4). El modelo proporcionó un buen ajuste tanto para los indicadores de incidencia semanal del HCoV-OC43 y el HCoV-HKU1 como para los números estimados de reproducción efectiva semanal ( Fig. 2 ). Según los parámetros del modelo de mejor ajuste, el R0 para HCoV-OC43 y HCoV-HKU1 varía entre 1.7 en el verano y 2.2 en el invierno, y los picos en la segunda semana de enero en acuerdo con la horquilla estacional estimada a partir de los datos. Además, de acuerdo a los resultados de este modelo de regresión SEIRS, se estima que la duración de la inmunidad para ambas cepas es de aproximadamente 45 semanas, y que cada cepa induce inmunidad cruzada contra la otra cepa. Finalmente se ve que la inmunidad cruzada que HCoV-OC43 induce contra HCoV-HKU1 es más fuerte que la contraria.
Fig. 1 Efectos de la reducción de la población susceptible y la estacionalidad sobre el número efectivo de reproducción por cepa y temporada.Efectos multiplicativos estimados de la incidencia de HCoV-HKU1 (rojo), incidencia de HCoV-OC43 (azul) y factor estacional (oro) sobre los números de reproducción efectiva semanal de HCoV-HKU1 (paneles superiores) y HCoV-OC43 (abajo), con intervalos de confianza del 95%. El punto negro (con un intervalo de confianza del 95%) trazado al comienzo de cada temporada es el coeficiente estimado para esa cepa y temporada en comparación con la temporada 2014-15 HCoV-HKU1. La horquilla del factor estacional se establece en 1 en la primera semana de la temporada (sin impedimentos). En el eje x, la primera "semana en la temporada" corresponde a la semana epidemiológica 40.Integramos estos hallazgos en un modelo compartimental de dos cepas usando las ecuaciones diferenciales ordinarias (EDO) del modelo epidemilógico: susceptible-expuesto-infeccioso-recuperado-susceptible (SEIRS) para describir la dinámica de transmisión de HCoV-OC43 y HCoV-HKU1 (fig. S4). El modelo proporcionó un buen ajuste tanto para los indicadores de incidencia semanal del HCoV-OC43 y el HCoV-HKU1 como para los números estimados de reproducción efectiva semanal ( Fig. 2 ). Según los parámetros del modelo de mejor ajuste, el R0 para HCoV-OC43 y HCoV-HKU1 varía entre 1.7 en el verano y 2.2 en el invierno, y los picos en la segunda semana de enero en acuerdo con la horquilla estacional estimada a partir de los datos. Además, de acuerdo a los resultados de este modelo de regresión SEIRS, se estima que la duración de la inmunidad para ambas cepas es de aproximadamente 45 semanas, y que cada cepa induce inmunidad cruzada contra la otra cepa. Finalmente se ve que la inmunidad cruzada que HCoV-OC43 induce contra HCoV-HKU1 es más fuerte que la contraria. Fig. 2 Modelo de transmisión para el HCoV-OC43 y HCoV-HKU1.( A ) Comparación del porcentaje de pruebas de laboratorio positivas por semana multiplicadas por el porcentaje de enfermedades similares a la influenza (ILI) para los betacoronavirus humanos HCoV-OC43 (azul) y HCoV-HKU1 (rojo) en los Estados Unidos entre el 5 de julio de 2014 y el 29 de junio de 2019 (líneas continuas), con la salida simulada del modelo de transmisión SEIRS de mejor ajuste (líneas discontinuas). ( B y C ) Números de reproducción efectivos semanales ( Re ) estimados usando el método de Wallinga-Teunis (puntos) frente al Re resultado de usar el mejor modelo de transmisión SEIRS (línea) para HCoVs OC43 y HKU1. La opacidad de cada punto está determinada por el porcentaje relativo de ILI multiplicado por el porcentaje de pruebas de laboratorio positivas en esa semana en relación con el porcentaje máximo de ILI, multiplicado por el porcentaje de pruebas de laboratorio positivas para esa cepa durante el período de estudio, lo que refleja la incertidumbre en la estimación de Re. Las estimaciones son más certeras (puntos más oscuros) en las semanas con mayor incidencia.Simulando la transmisión de SARS-CoV-2A continuación, incorporamos un tercer betacoronavirus en este modelo de transmisión dinámica para representar al SARS-CoV-2. Asumimos un periodo de latencia de 4,6 días ( 26 , 37 - 39 ) y un período infeccioso de 5 días utilizando los valores de mejor ajuste para otros betacoronavirus (tabla S8). Permitimos en este estudio que las inmunidades cruzadas, la duración de la inmunidad, el máximo R0 y el grado de variación estacional en R0 varíen. Asumimos un tiempo de establecimiento de transmisión sostenida dedsde el 11 de marzo de 2020, cuando la Organización Mundial de la Salud declaró el brote de SARS-CoV-2 como una pandemia ( 40). Para un conjunto representativo de valores de todos estos parámetros, medimos las posibles infecciones anuales por SARS-CoV-2 (tablas S2 a S4 y fig. S7) así como la prevalencia anual máxima de SARS-CoV-2 (tablas S5 a S7 y fig. S7) hasta el año 2025. Finalmente resumimos esta dinámica post-pandémica del SARS-CoV-2 en las categorías de brotes anuales, brotes bienales, brotes esporádicos o eliminación total (tablas S2 a S7). Comentar que, en general, duraciones más cortas de la inmunidad y grados más pequeños de inmunidad cruzada hacia los otros betacoronavirus se asociaron con una mayor incidencia total de la infección debida al SARS-CoV-2, mientras que los repuntes en otoño y fluctuaciones estacionales pequeñas se asociaron con picos de pandemia más grandes. Las simulaciones del modelo demostraron los siguientes puntos clave:El SARS-CoV-2 puede proliferar en cualquier época del año.En todos los escenarios modelados, el SARS-CoV-2 fue capaz de producir un brote sustancial independientemente del tiempo de establecimiento. Los establecimientos de invierno / primavera favorecieron los brotes con picos más bajos, mientras que los establecimientos de otoño / invierno condujeron a brotes más agudos (tablas S2 a S4 y fig. S7). Los indicadores de incidencia acumulada a cinco años fueron comparables para todos casos (tablas S2 a S4).Si la inmunidad al SARS-CoV-2 no es permanente, es probable que entre en circulación regularAl igual que la influenza pandémica, muchos escenarios conducen a que el SARS-CoV-2 entre en circulación a largo plazo junto con otros betacoronavirus humanos ( Fig. 3, A y B ), posiblemente en patrones anuales, bienales o esporádicos durante los próximos cinco años (tablas S2 a S4). La inmunidad a corto plazo (del orden de 40 semanas, similar a HCoV-OC43 y HCoV-HKU1) favorece el establecimiento de brotes anuales de SARS-CoV-2, mientras que la inmunidad a largo plazo (dos años) favorece los brotes bienales.
Fig. 2 Modelo de transmisión para el HCoV-OC43 y HCoV-HKU1.( A ) Comparación del porcentaje de pruebas de laboratorio positivas por semana multiplicadas por el porcentaje de enfermedades similares a la influenza (ILI) para los betacoronavirus humanos HCoV-OC43 (azul) y HCoV-HKU1 (rojo) en los Estados Unidos entre el 5 de julio de 2014 y el 29 de junio de 2019 (líneas continuas), con la salida simulada del modelo de transmisión SEIRS de mejor ajuste (líneas discontinuas). ( B y C ) Números de reproducción efectivos semanales ( Re ) estimados usando el método de Wallinga-Teunis (puntos) frente al Re resultado de usar el mejor modelo de transmisión SEIRS (línea) para HCoVs OC43 y HKU1. La opacidad de cada punto está determinada por el porcentaje relativo de ILI multiplicado por el porcentaje de pruebas de laboratorio positivas en esa semana en relación con el porcentaje máximo de ILI, multiplicado por el porcentaje de pruebas de laboratorio positivas para esa cepa durante el período de estudio, lo que refleja la incertidumbre en la estimación de Re. Las estimaciones son más certeras (puntos más oscuros) en las semanas con mayor incidencia.Simulando la transmisión de SARS-CoV-2A continuación, incorporamos un tercer betacoronavirus en este modelo de transmisión dinámica para representar al SARS-CoV-2. Asumimos un periodo de latencia de 4,6 días ( 26 , 37 - 39 ) y un período infeccioso de 5 días utilizando los valores de mejor ajuste para otros betacoronavirus (tabla S8). Permitimos en este estudio que las inmunidades cruzadas, la duración de la inmunidad, el máximo R0 y el grado de variación estacional en R0 varíen. Asumimos un tiempo de establecimiento de transmisión sostenida dedsde el 11 de marzo de 2020, cuando la Organización Mundial de la Salud declaró el brote de SARS-CoV-2 como una pandemia ( 40). Para un conjunto representativo de valores de todos estos parámetros, medimos las posibles infecciones anuales por SARS-CoV-2 (tablas S2 a S4 y fig. S7) así como la prevalencia anual máxima de SARS-CoV-2 (tablas S5 a S7 y fig. S7) hasta el año 2025. Finalmente resumimos esta dinámica post-pandémica del SARS-CoV-2 en las categorías de brotes anuales, brotes bienales, brotes esporádicos o eliminación total (tablas S2 a S7). Comentar que, en general, duraciones más cortas de la inmunidad y grados más pequeños de inmunidad cruzada hacia los otros betacoronavirus se asociaron con una mayor incidencia total de la infección debida al SARS-CoV-2, mientras que los repuntes en otoño y fluctuaciones estacionales pequeñas se asociaron con picos de pandemia más grandes. Las simulaciones del modelo demostraron los siguientes puntos clave:El SARS-CoV-2 puede proliferar en cualquier época del año.En todos los escenarios modelados, el SARS-CoV-2 fue capaz de producir un brote sustancial independientemente del tiempo de establecimiento. Los establecimientos de invierno / primavera favorecieron los brotes con picos más bajos, mientras que los establecimientos de otoño / invierno condujeron a brotes más agudos (tablas S2 a S4 y fig. S7). Los indicadores de incidencia acumulada a cinco años fueron comparables para todos casos (tablas S2 a S4).Si la inmunidad al SARS-CoV-2 no es permanente, es probable que entre en circulación regularAl igual que la influenza pandémica, muchos escenarios conducen a que el SARS-CoV-2 entre en circulación a largo plazo junto con otros betacoronavirus humanos ( Fig. 3, A y B ), posiblemente en patrones anuales, bienales o esporádicos durante los próximos cinco años (tablas S2 a S4). La inmunidad a corto plazo (del orden de 40 semanas, similar a HCoV-OC43 y HCoV-HKU1) favorece el establecimiento de brotes anuales de SARS-CoV-2, mientras que la inmunidad a largo plazo (dos años) favorece los brotes bienales. Fig. 3 Distintos escenariosde prevalencia para el SARS-CoV-2 en regiones templadas durante los próximos cinco años.Estas gráficas representan la prevalencia del SARS-CoV-2 (negro, casos por 1,000 personas), HCoV-OC43 (azul,% positivo multiplicado por% ILI) y HCoV-HKU1 (rojo,% positivo multiplicado por% ILI) para un conjunto representativo de posibles escenarios de pandemia y post pandemia. Los escenarios se obtuvieron variando la inmunidad cruzada entre SARS-CoV-2 y HCoVs OC43 / HKU1 (χ 3X ) y viceversa (χ X3 ), variando la duración de la inmunidad de SARS-CoV-2 (1 / σ 3), y la variación estacional en R0 ( f ), y suponiendo un tiempo de establecimiento epidémico del 11 de marzo de 2020 (representado como una barra gris vertical). Los valores de los parámetros utilizados para generar cada gráfico se enumeran a continuación; todos los demás parámetros se mantuvieron en los valores enumerados en la tabla S8. ( A) Una corta duración (1 / σ 3 = 40 semanas) de inmunidad contra el SARS-CoV-2 podría producir brotes anuales de SARS-CoV-2. ( B ) La inmunidad a largo plazo del SARS-CoV-2 (1 / σ 3 = 104 semanas) podría producir brotes bienales, posiblemente con brotes más pequeños en los años intermedios. ( C ) Una mayor variación estacional en la transmisión ( f = 0.4) reduciría el tamaño máximo de la onda de infección, pero podría conducir a brotes de invierno más severos a partir de entonces [compárese con (B)]. ( D ) Si la inmunidad es de largo plazo (1 / σ 3 = infinito) se podría conducir a la eliminación del virus. ( E) Sin embargo, un resurgimiento del SARS-CoV-2 podría ocurrir tan tarde como en 2024 después de un período de eliminación aparente si la duración de la inmunidad es intermedia (1 / σ 3 = 104 semanas) y si los HCoVs OC43 / HKU1 imparten inmunidad cruzada intermedia contra SARS-CoV-2 (χ 3X = 0.3).(A) χ 3X = 0.3, χ X3 = 0, 1 / σ 3 = 40 semanas, f = 0.2. (B) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = 104 semanas, f = 0.2. (C) χ 3X = 0.7, χ X3 = 0, 1 / σ 3= 104 semanas, f = 0.4. (D) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = infinito, f = 0.2. (E) χ 3X = 0.3, χ X3 = 0.3, 1 / σ 3 = 104 semanas, f = 0.4.La alta variación estacional en la transmisión conduce a una menor incidencia máxima durante la onda pandémica inicial, pero a brotes recurrentes más grandes en inviernoLa cantidad de variación estacional en la transmisión del SARS-CoV-2 podría diferir entre ubicaciones geográficas, como en el caso de la influenza ( 12 ). La R0 para la influenza en Nueva York disminuye en el verano en aproximadamente un 40%, mientras que en Florida la disminución está más cerca del 20%, lo que se alinea con la disminución estimada en R0 para HCoV-OC43 y HCoV-HKU1 (tabla S8). Una disminución del 40% en el verano en R0 reduciría la incidencia máxima no mitigada de la onda pandémica inicial de SARS-CoV-2. Sin embargo, un factor estacional más fuerte conduce a una mayor acumulación de individuos susceptibles durante los períodos de baja transmisión en el verano, lo que lleva a brotes recurrentes con picos más altos en el período posterior a la pandemia ( Fig. 3C ).Si la inmunidad al SARS-CoV-2 es permanente, el virus podría desaparecer tras cinco años o más después de causar el actual broteLa inmunidad a largo plazo conduce consistentemente a la eliminación efectiva del SARS-CoV-2 y a una menor incidencia general de infección. Si el SARS-CoV-2 induce inmunidad cruzada contra HCoV-OC43 y HCoV-HKU1, la incidencia de todos los betacoronavirus podría disminuir e incluso desaparecer virtualmente ( Fig. 3D ). La eliminación virtual de HCoV-OC43 y HCoV-HKU1 sería posible si SARS-CoV-2 indujera un 70% de inmunidad cruzada contra ellos, que es el mismo nivel estimado de inmunidad cruzada que HCoV-OC43 induce contra HCoV-HKU1.Unos bajos niveles de inmunidad cruzada de los otros betacoronavirus contra el SARS-CoV-2 podrían hacer que el SARS-CoV-2 parezca extinguirse, solo para resurgir después de unos años.Incluso si la inmunidad contra el SARS-CoV-2 solo durase dos años, la inmunidad cruzada leve (30%) de HCoV-OC43 y HCoV-HKU1 podrían eliminar efectivamente la transmisión del SARS-CoV-2 hasta tres años antes de un resurgimiento en 2024, siempre que el SARS-CoV-2 no se extinga por completo ( Fig. 3E ).Para ilustrar estos escenarios ( Fig. 3 ), utilizamos un valor máximo en invierno de R0 = 2.2, a partir del valor R0 estimado para HCoV-OC43 y HCoV-HKU1 (tabla S8). Esta es una estimación baja pero plausible del número de reproducción básico para el SARS-CoV-2 ( 41 ). El aumento en invierno de R0 a 2.6 conduce a brotes más intensos, pero el rango cualitativo de escenarios sigue siendo similar (fig. S8).Evaluación de escenarios de intervención durante la ola pandémica inicialIndependientemente de la dinámica de transmisión pospandémica del SARS-CoV-2, se requieren medidas urgentes para abordar la epidemia en curso. Los tratamientos farmacéuticos y las vacunas pueden requerir meses o años para desarrollarse y probarse, dejando las intervenciones no farmacéuticas (NPI) como el único medio inmediato para frenar la transmisión del SARS-CoV-2. Se han adoptado medidas de distanciamiento social en muchos países con transmisión generalizada de SARS-CoV-2. La duración e intensidad necesarias de estas medidas aún no se han caracterizado. Para abordar esto, adaptamos el modelo de transmisión SEIRS (fig. S9) para capturar infecciones moderadas / leves / asintomáticas (95.6% de las infecciones), infecciones que conducen a la hospitalización pero no a una atención médica crítica (3.08% de las infecciones) e infecciones que requieren cuidados intensivos (1.32% de las infecciones) ( 26) Asumimos el peor de los casos de inmunidad cruzada de HCoV-OC43 y HCoV-HKU1 contra el SARS-CoV-2, lo que hace que el modelo de SARS-CoV-2 no se vea afectado por la dinámica de transmisión de estos virus. A partir de los ajustes del modelo de transmisión, asumimos un período latente de 4,6 días y un período infeccioso de 5 días, de acuerdo con las estimaciones de otros estudios ( 26 ). La duración media de la estancia hospitalaria no crítica fue de 8 días, y de 6 días para aquellos que sí requirieron de atención médica intensiva, y la duración media de dicha atención crítica fue de 10 días ( 26 ). Variamos el pico (invierno) de R0 entre 2.2 y 2.6, y permitimos que en verano R0 variase entre el 60% ( es decir; estacionalidad relativamente fuerte) y el 100% del R0 invernal (es decir, sin estacionalidad) guiados por el factor estacional inferido para el HCoV-OC43 y el HCoV-HKU1 (tabla S8).Utilizamos la capacidad de atención médica intensiva (UCI) de los Estados Unidos, 0.89 camas por cada 10,000 adultos, como punto de referencia para la demanda de atención crítica ( 2 ). Simulamos trayectorias epidémicas basadas en un tiempo de inicio epidémico en el 11 de marzo de 2020. Simulamos el distanciamiento social reduciendo R0 en una proporción fija, que oscila entre el 0 y el 60%. Evaluamos intervenciones de "distanciamiento social" únicas, para las cuales el R0 se redujo hasta en un 60% por un período fijo de tiempo (hasta 20 semanas), o de manera indefinida desde dos semanas después del establecimiento de la epidemia. También evaluamos medidas intermitentes de distanciamiento social, para las cuales el distanciamiento social se activa cuando la prevalencia de infección aumenta por encima de un cierto umbral y se desactiva cuando cae por debajo de un segundo umbral de cota inferior, con el objetivo de no saturar la capacidad de cuidados intensivos: i.e.; pacientes por debajo de 0.89 por 10,000 adultos. Un umbral para 'activar' de 35 casos por cada 10.000 personas logró este objetivo tanto en los casos estacionales como no estacionales con el invierno R0 = 2.2. Elegimos 5 casos por cada 10,000 adultos como el umbral para 'desactivar'. Estos umbrales fueron elegidos para ilustrar cualitativamente el escenario de intervención intermitente; en la práctica, los umbrales deberán ajustarse a la dinámica epidémica local y las capacidades hospitalarias. Realizamos un análisis de sensibilidad alrededor de estos valores umbrales (figs. S10 y S11) para evaluar cómo afectaron la duración y la frecuencia de las intervenciones. También implementamos un modelo con compartimentos adicionales para el período latente, el período infeccioso y cada período de hospitalización, de modo que los tiempos de espera en estos estados se distribuyeran siguiendo una distribución gamma en lugar de distribuirse exponencialmente (ver los materiales y métodos complementarios y las figuras S16 y S17) . Finalmente evaluamos el impacto de duplicar la capacidad de atención crítica (y los umbrales de activación / desactivación asociados) en la frecuencia y duración general de las medidas de distanciamiento social.Evaluamos el impacto de realizar un único periodo de distanciamiento social, variando la efectividad y duración en el pico y el momento de la epidemia, con y sin factor estacional importante. Cuando la transmisión no estaba sujeta al factor estacional, las medidas de distanciamiento social únicas redujeron el tamaño máximo de la epidemia ( Fig. 4 y Fig. S12); pero en todos los escenarios hubo un resurgimiento de la infección cuando se levantaron las medidas de distanciamiento social. Además, el distanciamiento social temporal más largo y más estricto no siempre se correlacionó con mayores reducciones en el tamaño máximo de la epidemia cuando vuelve a resurgir. En el caso de un período de 20 semanas de distanciamiento social con una reducción del 60% en R0, por ejemplo ( Fig. 4D), el tamaño máximo del pico de la epidemia al resurgir fue casi el mismo que el tamaño máximo de la epidemia no controlada: en otras palabras, el distanciamiento social fue tan efectivo que prácticamente no se construyó inmunidad poblacional. Las mayores reducciones en el tamaño máximo del pico provienen de casos donde la intensidad y la duración del distanciamiento social se dividen aproximadamente por igual entre los picos ( 42 ).
Fig. 3 Distintos escenariosde prevalencia para el SARS-CoV-2 en regiones templadas durante los próximos cinco años.Estas gráficas representan la prevalencia del SARS-CoV-2 (negro, casos por 1,000 personas), HCoV-OC43 (azul,% positivo multiplicado por% ILI) y HCoV-HKU1 (rojo,% positivo multiplicado por% ILI) para un conjunto representativo de posibles escenarios de pandemia y post pandemia. Los escenarios se obtuvieron variando la inmunidad cruzada entre SARS-CoV-2 y HCoVs OC43 / HKU1 (χ 3X ) y viceversa (χ X3 ), variando la duración de la inmunidad de SARS-CoV-2 (1 / σ 3), y la variación estacional en R0 ( f ), y suponiendo un tiempo de establecimiento epidémico del 11 de marzo de 2020 (representado como una barra gris vertical). Los valores de los parámetros utilizados para generar cada gráfico se enumeran a continuación; todos los demás parámetros se mantuvieron en los valores enumerados en la tabla S8. ( A) Una corta duración (1 / σ 3 = 40 semanas) de inmunidad contra el SARS-CoV-2 podría producir brotes anuales de SARS-CoV-2. ( B ) La inmunidad a largo plazo del SARS-CoV-2 (1 / σ 3 = 104 semanas) podría producir brotes bienales, posiblemente con brotes más pequeños en los años intermedios. ( C ) Una mayor variación estacional en la transmisión ( f = 0.4) reduciría el tamaño máximo de la onda de infección, pero podría conducir a brotes de invierno más severos a partir de entonces [compárese con (B)]. ( D ) Si la inmunidad es de largo plazo (1 / σ 3 = infinito) se podría conducir a la eliminación del virus. ( E) Sin embargo, un resurgimiento del SARS-CoV-2 podría ocurrir tan tarde como en 2024 después de un período de eliminación aparente si la duración de la inmunidad es intermedia (1 / σ 3 = 104 semanas) y si los HCoVs OC43 / HKU1 imparten inmunidad cruzada intermedia contra SARS-CoV-2 (χ 3X = 0.3).(A) χ 3X = 0.3, χ X3 = 0, 1 / σ 3 = 40 semanas, f = 0.2. (B) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = 104 semanas, f = 0.2. (C) χ 3X = 0.7, χ X3 = 0, 1 / σ 3= 104 semanas, f = 0.4. (D) χ 3X = 0.7, χ X3 = 0, 1 / σ 3 = infinito, f = 0.2. (E) χ 3X = 0.3, χ X3 = 0.3, 1 / σ 3 = 104 semanas, f = 0.4.La alta variación estacional en la transmisión conduce a una menor incidencia máxima durante la onda pandémica inicial, pero a brotes recurrentes más grandes en inviernoLa cantidad de variación estacional en la transmisión del SARS-CoV-2 podría diferir entre ubicaciones geográficas, como en el caso de la influenza ( 12 ). La R0 para la influenza en Nueva York disminuye en el verano en aproximadamente un 40%, mientras que en Florida la disminución está más cerca del 20%, lo que se alinea con la disminución estimada en R0 para HCoV-OC43 y HCoV-HKU1 (tabla S8). Una disminución del 40% en el verano en R0 reduciría la incidencia máxima no mitigada de la onda pandémica inicial de SARS-CoV-2. Sin embargo, un factor estacional más fuerte conduce a una mayor acumulación de individuos susceptibles durante los períodos de baja transmisión en el verano, lo que lleva a brotes recurrentes con picos más altos en el período posterior a la pandemia ( Fig. 3C ).Si la inmunidad al SARS-CoV-2 es permanente, el virus podría desaparecer tras cinco años o más después de causar el actual broteLa inmunidad a largo plazo conduce consistentemente a la eliminación efectiva del SARS-CoV-2 y a una menor incidencia general de infección. Si el SARS-CoV-2 induce inmunidad cruzada contra HCoV-OC43 y HCoV-HKU1, la incidencia de todos los betacoronavirus podría disminuir e incluso desaparecer virtualmente ( Fig. 3D ). La eliminación virtual de HCoV-OC43 y HCoV-HKU1 sería posible si SARS-CoV-2 indujera un 70% de inmunidad cruzada contra ellos, que es el mismo nivel estimado de inmunidad cruzada que HCoV-OC43 induce contra HCoV-HKU1.Unos bajos niveles de inmunidad cruzada de los otros betacoronavirus contra el SARS-CoV-2 podrían hacer que el SARS-CoV-2 parezca extinguirse, solo para resurgir después de unos años.Incluso si la inmunidad contra el SARS-CoV-2 solo durase dos años, la inmunidad cruzada leve (30%) de HCoV-OC43 y HCoV-HKU1 podrían eliminar efectivamente la transmisión del SARS-CoV-2 hasta tres años antes de un resurgimiento en 2024, siempre que el SARS-CoV-2 no se extinga por completo ( Fig. 3E ).Para ilustrar estos escenarios ( Fig. 3 ), utilizamos un valor máximo en invierno de R0 = 2.2, a partir del valor R0 estimado para HCoV-OC43 y HCoV-HKU1 (tabla S8). Esta es una estimación baja pero plausible del número de reproducción básico para el SARS-CoV-2 ( 41 ). El aumento en invierno de R0 a 2.6 conduce a brotes más intensos, pero el rango cualitativo de escenarios sigue siendo similar (fig. S8).Evaluación de escenarios de intervención durante la ola pandémica inicialIndependientemente de la dinámica de transmisión pospandémica del SARS-CoV-2, se requieren medidas urgentes para abordar la epidemia en curso. Los tratamientos farmacéuticos y las vacunas pueden requerir meses o años para desarrollarse y probarse, dejando las intervenciones no farmacéuticas (NPI) como el único medio inmediato para frenar la transmisión del SARS-CoV-2. Se han adoptado medidas de distanciamiento social en muchos países con transmisión generalizada de SARS-CoV-2. La duración e intensidad necesarias de estas medidas aún no se han caracterizado. Para abordar esto, adaptamos el modelo de transmisión SEIRS (fig. S9) para capturar infecciones moderadas / leves / asintomáticas (95.6% de las infecciones), infecciones que conducen a la hospitalización pero no a una atención médica crítica (3.08% de las infecciones) e infecciones que requieren cuidados intensivos (1.32% de las infecciones) ( 26) Asumimos el peor de los casos de inmunidad cruzada de HCoV-OC43 y HCoV-HKU1 contra el SARS-CoV-2, lo que hace que el modelo de SARS-CoV-2 no se vea afectado por la dinámica de transmisión de estos virus. A partir de los ajustes del modelo de transmisión, asumimos un período latente de 4,6 días y un período infeccioso de 5 días, de acuerdo con las estimaciones de otros estudios ( 26 ). La duración media de la estancia hospitalaria no crítica fue de 8 días, y de 6 días para aquellos que sí requirieron de atención médica intensiva, y la duración media de dicha atención crítica fue de 10 días ( 26 ). Variamos el pico (invierno) de R0 entre 2.2 y 2.6, y permitimos que en verano R0 variase entre el 60% ( es decir; estacionalidad relativamente fuerte) y el 100% del R0 invernal (es decir, sin estacionalidad) guiados por el factor estacional inferido para el HCoV-OC43 y el HCoV-HKU1 (tabla S8).Utilizamos la capacidad de atención médica intensiva (UCI) de los Estados Unidos, 0.89 camas por cada 10,000 adultos, como punto de referencia para la demanda de atención crítica ( 2 ). Simulamos trayectorias epidémicas basadas en un tiempo de inicio epidémico en el 11 de marzo de 2020. Simulamos el distanciamiento social reduciendo R0 en una proporción fija, que oscila entre el 0 y el 60%. Evaluamos intervenciones de "distanciamiento social" únicas, para las cuales el R0 se redujo hasta en un 60% por un período fijo de tiempo (hasta 20 semanas), o de manera indefinida desde dos semanas después del establecimiento de la epidemia. También evaluamos medidas intermitentes de distanciamiento social, para las cuales el distanciamiento social se activa cuando la prevalencia de infección aumenta por encima de un cierto umbral y se desactiva cuando cae por debajo de un segundo umbral de cota inferior, con el objetivo de no saturar la capacidad de cuidados intensivos: i.e.; pacientes por debajo de 0.89 por 10,000 adultos. Un umbral para 'activar' de 35 casos por cada 10.000 personas logró este objetivo tanto en los casos estacionales como no estacionales con el invierno R0 = 2.2. Elegimos 5 casos por cada 10,000 adultos como el umbral para 'desactivar'. Estos umbrales fueron elegidos para ilustrar cualitativamente el escenario de intervención intermitente; en la práctica, los umbrales deberán ajustarse a la dinámica epidémica local y las capacidades hospitalarias. Realizamos un análisis de sensibilidad alrededor de estos valores umbrales (figs. S10 y S11) para evaluar cómo afectaron la duración y la frecuencia de las intervenciones. También implementamos un modelo con compartimentos adicionales para el período latente, el período infeccioso y cada período de hospitalización, de modo que los tiempos de espera en estos estados se distribuyeran siguiendo una distribución gamma en lugar de distribuirse exponencialmente (ver los materiales y métodos complementarios y las figuras S16 y S17) . Finalmente evaluamos el impacto de duplicar la capacidad de atención crítica (y los umbrales de activación / desactivación asociados) en la frecuencia y duración general de las medidas de distanciamiento social.Evaluamos el impacto de realizar un único periodo de distanciamiento social, variando la efectividad y duración en el pico y el momento de la epidemia, con y sin factor estacional importante. Cuando la transmisión no estaba sujeta al factor estacional, las medidas de distanciamiento social únicas redujeron el tamaño máximo de la epidemia ( Fig. 4 y Fig. S12); pero en todos los escenarios hubo un resurgimiento de la infección cuando se levantaron las medidas de distanciamiento social. Además, el distanciamiento social temporal más largo y más estricto no siempre se correlacionó con mayores reducciones en el tamaño máximo de la epidemia cuando vuelve a resurgir. En el caso de un período de 20 semanas de distanciamiento social con una reducción del 60% en R0, por ejemplo ( Fig. 4D), el tamaño máximo del pico de la epidemia al resurgir fue casi el mismo que el tamaño máximo de la epidemia no controlada: en otras palabras, el distanciamiento social fue tan efectivo que prácticamente no se construyó inmunidad poblacional. Las mayores reducciones en el tamaño máximo del pico provienen de casos donde la intensidad y la duración del distanciamiento social se dividen aproximadamente por igual entre los picos ( 42 ). Fig. 4 Escenarios de distanciamiento social únicos en ausencia de estacionalidad.( A a E ) Prevalencia simulada de infecciones por COVID-19 (sólido) y casos críticos de COVID-19 (discontinuo) después del establecimiento el 11 de marzo de 2020 de un único período de distanciamiento social (región azul sombreada) instaladas dos semanas después. Variamos la duración de distanciamiento social (único) duradero en (A) cuatro semanas, (B) ocho semanas, (C) doce semanas, (D) veinte semanas y (E) indefinidamente. No hay forzamiento estacional; R 0 se mantuvo constante en 2.2 (ver fig. S12 para R 0 = 2.6). La efectividad del distanciamiento social varió de ninguna a una reducción del 60% en R 0 . Los tamaños de infección acumulados se representan junto a cada gráfico de prevalencia ( F a J) con el umbral de inmunidad del rebaño (barra negra horizontal). De los escenarios de distanciamiento temporal, el distanciamiento social a largo plazo (20 semanas), moderadamente efectivo (20% -40%) produce el pico global más pequeño y el tamaño total del brote.Para simulaciones con forzamiento estacional, el pico resurgimiento posterior a la intervención podría exceder el tamaño de la epidemia sin restricciones ( Fig. 5 y Fig. S13), tanto en términos de prevalencia pico como en términos de número total de infectados. El fuerte distanciamiento social mantuvo una alta proporción de individuos susceptibles en la población, lo que condujo a una epidemia intensa cuando R 0 aumenta a fines del otoño y el invierno. Ninguna de las intervenciones únicas fue efectiva para mantener la prevalencia de casos críticos por debajo de la capacidad de cuidados críticos.
Fig. 4 Escenarios de distanciamiento social únicos en ausencia de estacionalidad.( A a E ) Prevalencia simulada de infecciones por COVID-19 (sólido) y casos críticos de COVID-19 (discontinuo) después del establecimiento el 11 de marzo de 2020 de un único período de distanciamiento social (región azul sombreada) instaladas dos semanas después. Variamos la duración de distanciamiento social (único) duradero en (A) cuatro semanas, (B) ocho semanas, (C) doce semanas, (D) veinte semanas y (E) indefinidamente. No hay forzamiento estacional; R 0 se mantuvo constante en 2.2 (ver fig. S12 para R 0 = 2.6). La efectividad del distanciamiento social varió de ninguna a una reducción del 60% en R 0 . Los tamaños de infección acumulados se representan junto a cada gráfico de prevalencia ( F a J) con el umbral de inmunidad del rebaño (barra negra horizontal). De los escenarios de distanciamiento temporal, el distanciamiento social a largo plazo (20 semanas), moderadamente efectivo (20% -40%) produce el pico global más pequeño y el tamaño total del brote.Para simulaciones con forzamiento estacional, el pico resurgimiento posterior a la intervención podría exceder el tamaño de la epidemia sin restricciones ( Fig. 5 y Fig. S13), tanto en términos de prevalencia pico como en términos de número total de infectados. El fuerte distanciamiento social mantuvo una alta proporción de individuos susceptibles en la población, lo que condujo a una epidemia intensa cuando R 0 aumenta a fines del otoño y el invierno. Ninguna de las intervenciones únicas fue efectiva para mantener la prevalencia de casos críticos por debajo de la capacidad de cuidados críticos. Fig. 5 Escenarios de distanciamiento social únicos con factor estacional importante.( A a E ) Prevalencia simulada suponiendo un fuerte forzamiento estacional (invierno R0 = 2.2, verano R0 = 1.3, o disminución del 40%), de infecciones por COVID-19 (sólido) y casos críticos de COVID-19 (discontinuo) después del establecimiento el 11 de marzo de 2020 de un período único de distanciamiento social (región azul sombreada) instaladas dos semanas más tarde, variando la duración del distanciamiento social en (A) cuatro semanas, (B) ocho semanas, (C) doce semanas, (D) veinte semanas , y (E) indefinidamente (ver la figura S13 para un escenario con invierno R0 = 2.6). La efectividad del distanciamiento social la variamos de 0 (ninguna intervención) a una reducción del 60% en R0. Los tamaños de infección acumulados se representan junto a cada parcela de prevalencia ( F a J ) con el umbral de inmunidad poblacional (barra negra horizontal). La prevención de una infección generalizada durante el verano puede aplanar y prolongar la epidemia, pero también puede conducir a una alta densidad de individuos susceptibles que podrían infectarse en una intensa ola de otoño.El distanciamiento social intermitente podría evitar que se exceda la capacidad de cuidados críticos ( Fig. 6 y Fig. S14). Debido a la historia natural de la infección, hay un retraso de aproximadamente 3 semanas entre el inicio del distanciamiento social y la demanda máxima de cuidados intensivos. Cuando la transmisión se ve forzada estacionalmente, el distanciamiento social en verano puede ser menos frecuente que cuando R0 permanece constante en su valor máximo de invierno durante todo el año. El período de tiempo entre las medidas de distanciamiento aumenta a medida que continúa la epidemia, ya que la acumulación de inmunidad en la población ralentiza el resurgimiento de la infección. Sin embargo, bajo las capacidades actuales de cuidados intensivos, la duración total de la epidemia de SARS-CoV-2 podría durar hasta 2022, lo que requeriría que se establecieran medidas de distanciamiento social entre el 25% (si hay estacionalidad y con un invierno donde R0 = 2; fig. S11A) y el 75% (sin estacionalidad y con un invierno donde R0 = 2.6; fig. S9C) de este intervalo de tiempo (desde ahora hasta el 2022). Cuando los períodos latentes, infecciosos y de hospitalización están distribuidos por una distribución gamma, la incidencia aumenta más rápidamente, lo que requiere un umbral más bajo para implementar medidas de distanciamiento (25 casos por cada 10,000 individuos para R0 = 2.2 en nuestro modelo) e intervenciones más frecuentes (fig. S16).
Fig. 5 Escenarios de distanciamiento social únicos con factor estacional importante.( A a E ) Prevalencia simulada suponiendo un fuerte forzamiento estacional (invierno R0 = 2.2, verano R0 = 1.3, o disminución del 40%), de infecciones por COVID-19 (sólido) y casos críticos de COVID-19 (discontinuo) después del establecimiento el 11 de marzo de 2020 de un período único de distanciamiento social (región azul sombreada) instaladas dos semanas más tarde, variando la duración del distanciamiento social en (A) cuatro semanas, (B) ocho semanas, (C) doce semanas, (D) veinte semanas , y (E) indefinidamente (ver la figura S13 para un escenario con invierno R0 = 2.6). La efectividad del distanciamiento social la variamos de 0 (ninguna intervención) a una reducción del 60% en R0. Los tamaños de infección acumulados se representan junto a cada parcela de prevalencia ( F a J ) con el umbral de inmunidad poblacional (barra negra horizontal). La prevención de una infección generalizada durante el verano puede aplanar y prolongar la epidemia, pero también puede conducir a una alta densidad de individuos susceptibles que podrían infectarse en una intensa ola de otoño.El distanciamiento social intermitente podría evitar que se exceda la capacidad de cuidados críticos ( Fig. 6 y Fig. S14). Debido a la historia natural de la infección, hay un retraso de aproximadamente 3 semanas entre el inicio del distanciamiento social y la demanda máxima de cuidados intensivos. Cuando la transmisión se ve forzada estacionalmente, el distanciamiento social en verano puede ser menos frecuente que cuando R0 permanece constante en su valor máximo de invierno durante todo el año. El período de tiempo entre las medidas de distanciamiento aumenta a medida que continúa la epidemia, ya que la acumulación de inmunidad en la población ralentiza el resurgimiento de la infección. Sin embargo, bajo las capacidades actuales de cuidados intensivos, la duración total de la epidemia de SARS-CoV-2 podría durar hasta 2022, lo que requeriría que se establecieran medidas de distanciamiento social entre el 25% (si hay estacionalidad y con un invierno donde R0 = 2; fig. S11A) y el 75% (sin estacionalidad y con un invierno donde R0 = 2.6; fig. S9C) de este intervalo de tiempo (desde ahora hasta el 2022). Cuando los períodos latentes, infecciosos y de hospitalización están distribuidos por una distribución gamma, la incidencia aumenta más rápidamente, lo que requiere un umbral más bajo para implementar medidas de distanciamiento (25 casos por cada 10,000 individuos para R0 = 2.2 en nuestro modelo) e intervenciones más frecuentes (fig. S16). Fig. 6 Escenarios de distanciamiento social intermitentes con capacidad actual y ampliada de cuidados intensivos.Prevalencia de SARS-Cov-2 (curvas negras) y casos críticos (curvas rojas) bajo distanciamiento social intermitente (regiones azules sombreadas) sin factor estacional ( A y C ) y con factor estacional ( B y D ). Suponemos que el distanciamiento produce una reducción del 60% en R0. La capacidad máxima del cuidado intensivo está representada por las barras negras horizontales sólidas, y los umbrales de encendido / apagado para el distanciamiento social están representados por las líneas horizontales discontinuas. (A) y (B) son los escenarios con la capacidad actual de cuidados intensivos de EE.UU. Y (C) y (D) son los escenarios con el doble de la capacidad actual de cuidados intensivos. Seleccionamos para el invierno un máximo R0 de 2.2 y para los escenarios estacionales en verano el R0 es de 1.3 (disminución del 40%). La prevalencia está en negro y los casos de cuidados críticos están en rojo. A la derecha de cada parcela principal ( E a H ), la proporción inmune a lo largo del tiempo se representa en verde en relación al umbral de inmunidad poblacional (barra negra horizontal).El aumento de la capacidad de cuidados intensivos permitió que la inmunidad de la población se acumulara más rápidamente, reduciendo la duración total de la epidemia y la duración total de las medidas de distanciamiento social ( Fig. 6, C y D ). Si bien la frecuencia y la duración de las medidas de distanciamiento social fueron similares entre los escenarios con capacidad de atención crítica actual y ampliada, la epidemia finaliza en julio de 2022 y las medidas de distanciamiento social podrían relajarse por completo a principios o mediados de 2021 dependiendo nuevamente del grado de factor estacional de transmisión ( Fig. 6, C y D ). La introducción de un tratamiento hipotético que reduzca a la mitad la proporción de infecciones que requieren hospitalización tiene un efecto similar al de duplicar la capacidad de atención crítica (fig. S15).DiscusiónAquí examinamos una variedad de posibles escenarios de transmisión de SARS-CoV-2 hasta 2025 y evaluamos intervenciones no farmacéuticas que podrían mitigar la intensidad del brote actual. Si la inmunidad (anticuerpos) al SARS-CoV-2 disminuye en el tiempo de la misma manera que lo hace en otros coronavirus relacionados, es probable que ocurran brotes recurrentes durante el invierno en los próximos años. La incidencia total de SARS-CoV-2 hasta 2025 dependerá de manera crucial de esta duración en la inmunidad y, en menor grado, en la cantidad de inmunidad cruzada que exista entre HCoVs OC43 / HKU1 y el SARS-CoV-2. La intensidad de la onda pandémica actual dependerá fundamentalmente del número de reproducción básico R0 en el momento del establecimiento de la epidemia en cada país: si el establecimiento ocurre en otoño cuando el número de reproducción está aumentando, lo que podría ocurrir en países que mantengan un control de epidemias mediante rastreo de contactos y cuarentena durante el verano, o si el SARS-CoV-2 no está sujeto a la misma disminución de contagios en verano que demuestran HCoV-OC43 y HCoV-HKU1, entonces una alta prevalencia máxima de la infección es probable. Los esfuerzos de distanciamiento social únicos pueden empujar el pico epidémico del SARS-CoV-2 hasta el otoño, lo que puede exacerbar aún más la carga de los recursos de cuidados intensivos si resulta que aumenta su transmisibilidad durante el invierno. El distanciamiento social intermitente podría mantener la demanda de cuidados críticos dentro de los umbrales actuales, pero se requerirá una vigilancia generalizada para cronometrar las medidas de distanciamiento correctamente y evitar exceder la capacidad de cuidados intensivos. Nuevas terapias y/o vacunas,(43) podrían aliviar la necesidad de un distanciamiento social intermitente estricto para mantener el control de la epidemia. En ausencia de tales intervenciones, la vigilancia y el distanciamiento intermitente (o el distanciamiento sostenido si es necesario) podrían necesitar mantenerse hasta el 2022, lo que representaría una carga social y económica sustancial. Para acortar la epidemia de SARS-CoV-2 y garantizar una atención adecuada para los pacientes críticos, aumentar la capacidad de atención intensiva y desarrollar intervenciones adicionales son prioridades urgentes. Mientras tanto, se requieren pruebas serológicas masivas para comprender el alcance y la duración de la inmunidad natural (anticuerpos) al SARS-CoV-2, lo cual ayudará a determinar la dinámica pospandémica del virus. Se necesitará una vigilancia sostenida y generalizada tanto a corto plazo, para implementar eficazmente medidas de distanciamiento social intermitentes, como a largo plazo, para evaluar la posibilidad de resurgimientos de la infección por SARS-CoV-2, que podría ocurrir hasta el año 2025 incluso después de un período prolongado de aparente eliminación.Nuestras observaciones son consistentes con otras predicciones de cómo podría desarrollarse la transmisión del SARS-CoV-2 y con evaluaciones de los esfuerzos de mitigación que podrían ser necesarios para frenar el brote actual. Un reciente estudio que utilizó datos de Suecia encontró que el establecimiento estacional de la transmisión del SARS-CoV-2 es probable en el período posterior a la pandemia actual ( 11 ). Estudios observacionales y de modelación ( 2 , 26 ) demostraron que la implementación temprana de un fuerte distanciamiento social es esencial para controlar la propagación del SARS-CoV-2 y que, en ausencia del desarrollo de nuevas terapias o medidas preventivas como la búsqueda intensiva de casos confirmados y su posterior puesta en cuarentena obligatoria ( 21), las medidas de distanciamiento intermitente pueden ser la única forma de evitar una abrumadora capacidad de cuidados críticos mientras se consolida la inmunidad de la población. La observación de que un distanciamiento social fuerte y temporal puede conducir a resurgimientos especialmente grandes concuerda con los datos de la pandemia de influenza de 1918 en los Estados Unidos ( 44 ), en la cual el tamaño del pico de infección del otoño de 1918 se asoció inversamente con el del invierno posterior una vez que las intervenciones se relajaron.Nuestro estudio estuvo sujeto a ciertas limitaciones. Solo tuvimos disponibles cinco temporadas de datos de observación sobre los betacoronavirus, aunque los patrones de incidencia se parecen mucho a los de los 10 años anteriores comparados con los datos de un hospital en Suecia ( 11). Asumimos que los coeficientes utilizados fueron constantes en todas las estaciones, aunque el factor estacional probablemente difería de un año a otro en función de otros factores subyacentes. Para evitar que el modelo de transmisión se volviese excesivamente complejo, asumimos que no hubo diferencia en el factor estacional, la fuerza de infección por caso, el período latente o el período infeccioso entre los betacoronavirus. Sin embargo, nuestras estimaciones para estos valores se encuentran dentro de los rangos de estimaciones de la literatura vigente. Aunque la dinámica de la enfermedad puede variar según la edad, no teníamos datos suficientes para parametrizar un modelo estructurado por edad. Tampoco modelamos directamente ningún efecto de la apertura de escuelas, lo que podría conducir a un impulso adicional en la fuerza de transmisión a principios de otoño ( 45). El modelo de transmisión es determinista, por lo que no puede capturar la posibilidad de extinción del SARS-CoV-2. Tampoco incorpora estructura geográfica, por lo que no se puede evaluar la posibilidad de una transmisión espacialmente heterogénea. La construcción de modelos espacialmente explícitos serán más factible a medida que haya más datos disponibles sobre la incidencia de SARS-CoV-2. Esto ayudará a determinar si existen diferencias en el factor estacional entre ubicaciones geográficas, como en el caso de la influenza ( 12 ), y también ayudará a evaluar la posibilidad o no de la extinción epidémica al tener en cuenta las re-introducciones (casos importados). El momento y la intensidad de los brotes pospandémicos también pueden depender de estos casos importados, que pueden evaluarse utilizando modelos más complejos y globales.Utilizamos el porcentaje de prueba positiva multiplicado por el porcentaje de ILI para aproximar la incidencia de coronavirus hasta una constante proporcion
Fig. 6 Escenarios de distanciamiento social intermitentes con capacidad actual y ampliada de cuidados intensivos.Prevalencia de SARS-Cov-2 (curvas negras) y casos críticos (curvas rojas) bajo distanciamiento social intermitente (regiones azules sombreadas) sin factor estacional ( A y C ) y con factor estacional ( B y D ). Suponemos que el distanciamiento produce una reducción del 60% en R0. La capacidad máxima del cuidado intensivo está representada por las barras negras horizontales sólidas, y los umbrales de encendido / apagado para el distanciamiento social están representados por las líneas horizontales discontinuas. (A) y (B) son los escenarios con la capacidad actual de cuidados intensivos de EE.UU. Y (C) y (D) son los escenarios con el doble de la capacidad actual de cuidados intensivos. Seleccionamos para el invierno un máximo R0 de 2.2 y para los escenarios estacionales en verano el R0 es de 1.3 (disminución del 40%). La prevalencia está en negro y los casos de cuidados críticos están en rojo. A la derecha de cada parcela principal ( E a H ), la proporción inmune a lo largo del tiempo se representa en verde en relación al umbral de inmunidad poblacional (barra negra horizontal).El aumento de la capacidad de cuidados intensivos permitió que la inmunidad de la población se acumulara más rápidamente, reduciendo la duración total de la epidemia y la duración total de las medidas de distanciamiento social ( Fig. 6, C y D ). Si bien la frecuencia y la duración de las medidas de distanciamiento social fueron similares entre los escenarios con capacidad de atención crítica actual y ampliada, la epidemia finaliza en julio de 2022 y las medidas de distanciamiento social podrían relajarse por completo a principios o mediados de 2021 dependiendo nuevamente del grado de factor estacional de transmisión ( Fig. 6, C y D ). La introducción de un tratamiento hipotético que reduzca a la mitad la proporción de infecciones que requieren hospitalización tiene un efecto similar al de duplicar la capacidad de atención crítica (fig. S15).DiscusiónAquí examinamos una variedad de posibles escenarios de transmisión de SARS-CoV-2 hasta 2025 y evaluamos intervenciones no farmacéuticas que podrían mitigar la intensidad del brote actual. Si la inmunidad (anticuerpos) al SARS-CoV-2 disminuye en el tiempo de la misma manera que lo hace en otros coronavirus relacionados, es probable que ocurran brotes recurrentes durante el invierno en los próximos años. La incidencia total de SARS-CoV-2 hasta 2025 dependerá de manera crucial de esta duración en la inmunidad y, en menor grado, en la cantidad de inmunidad cruzada que exista entre HCoVs OC43 / HKU1 y el SARS-CoV-2. La intensidad de la onda pandémica actual dependerá fundamentalmente del número de reproducción básico R0 en el momento del establecimiento de la epidemia en cada país: si el establecimiento ocurre en otoño cuando el número de reproducción está aumentando, lo que podría ocurrir en países que mantengan un control de epidemias mediante rastreo de contactos y cuarentena durante el verano, o si el SARS-CoV-2 no está sujeto a la misma disminución de contagios en verano que demuestran HCoV-OC43 y HCoV-HKU1, entonces una alta prevalencia máxima de la infección es probable. Los esfuerzos de distanciamiento social únicos pueden empujar el pico epidémico del SARS-CoV-2 hasta el otoño, lo que puede exacerbar aún más la carga de los recursos de cuidados intensivos si resulta que aumenta su transmisibilidad durante el invierno. El distanciamiento social intermitente podría mantener la demanda de cuidados críticos dentro de los umbrales actuales, pero se requerirá una vigilancia generalizada para cronometrar las medidas de distanciamiento correctamente y evitar exceder la capacidad de cuidados intensivos. Nuevas terapias y/o vacunas,(43) podrían aliviar la necesidad de un distanciamiento social intermitente estricto para mantener el control de la epidemia. En ausencia de tales intervenciones, la vigilancia y el distanciamiento intermitente (o el distanciamiento sostenido si es necesario) podrían necesitar mantenerse hasta el 2022, lo que representaría una carga social y económica sustancial. Para acortar la epidemia de SARS-CoV-2 y garantizar una atención adecuada para los pacientes críticos, aumentar la capacidad de atención intensiva y desarrollar intervenciones adicionales son prioridades urgentes. Mientras tanto, se requieren pruebas serológicas masivas para comprender el alcance y la duración de la inmunidad natural (anticuerpos) al SARS-CoV-2, lo cual ayudará a determinar la dinámica pospandémica del virus. Se necesitará una vigilancia sostenida y generalizada tanto a corto plazo, para implementar eficazmente medidas de distanciamiento social intermitentes, como a largo plazo, para evaluar la posibilidad de resurgimientos de la infección por SARS-CoV-2, que podría ocurrir hasta el año 2025 incluso después de un período prolongado de aparente eliminación.Nuestras observaciones son consistentes con otras predicciones de cómo podría desarrollarse la transmisión del SARS-CoV-2 y con evaluaciones de los esfuerzos de mitigación que podrían ser necesarios para frenar el brote actual. Un reciente estudio que utilizó datos de Suecia encontró que el establecimiento estacional de la transmisión del SARS-CoV-2 es probable en el período posterior a la pandemia actual ( 11 ). Estudios observacionales y de modelación ( 2 , 26 ) demostraron que la implementación temprana de un fuerte distanciamiento social es esencial para controlar la propagación del SARS-CoV-2 y que, en ausencia del desarrollo de nuevas terapias o medidas preventivas como la búsqueda intensiva de casos confirmados y su posterior puesta en cuarentena obligatoria ( 21), las medidas de distanciamiento intermitente pueden ser la única forma de evitar una abrumadora capacidad de cuidados críticos mientras se consolida la inmunidad de la población. La observación de que un distanciamiento social fuerte y temporal puede conducir a resurgimientos especialmente grandes concuerda con los datos de la pandemia de influenza de 1918 en los Estados Unidos ( 44 ), en la cual el tamaño del pico de infección del otoño de 1918 se asoció inversamente con el del invierno posterior una vez que las intervenciones se relajaron.Nuestro estudio estuvo sujeto a ciertas limitaciones. Solo tuvimos disponibles cinco temporadas de datos de observación sobre los betacoronavirus, aunque los patrones de incidencia se parecen mucho a los de los 10 años anteriores comparados con los datos de un hospital en Suecia ( 11). Asumimos que los coeficientes utilizados fueron constantes en todas las estaciones, aunque el factor estacional probablemente difería de un año a otro en función de otros factores subyacentes. Para evitar que el modelo de transmisión se volviese excesivamente complejo, asumimos que no hubo diferencia en el factor estacional, la fuerza de infección por caso, el período latente o el período infeccioso entre los betacoronavirus. Sin embargo, nuestras estimaciones para estos valores se encuentran dentro de los rangos de estimaciones de la literatura vigente. Aunque la dinámica de la enfermedad puede variar según la edad, no teníamos datos suficientes para parametrizar un modelo estructurado por edad. Tampoco modelamos directamente ningún efecto de la apertura de escuelas, lo que podría conducir a un impulso adicional en la fuerza de transmisión a principios de otoño ( 45). El modelo de transmisión es determinista, por lo que no puede capturar la posibilidad de extinción del SARS-CoV-2. Tampoco incorpora estructura geográfica, por lo que no se puede evaluar la posibilidad de una transmisión espacialmente heterogénea. La construcción de modelos espacialmente explícitos serán más factible a medida que haya más datos disponibles sobre la incidencia de SARS-CoV-2. Esto ayudará a determinar si existen diferencias en el factor estacional entre ubicaciones geográficas, como en el caso de la influenza ( 12 ), y también ayudará a evaluar la posibilidad o no de la extinción epidémica al tener en cuenta las re-introducciones (casos importados). El momento y la intensidad de los brotes pospandémicos también pueden depender de estos casos importados, que pueden evaluarse utilizando modelos más complejos y globales.Utilizamos el porcentaje de prueba positiva multiplicado por el porcentaje de ILI para aproximar la incidencia de coronavirus hasta una constante proporcion
Cuando hacer deporte se vuelve delito
Os cuento algo personal que puede dar una pista del mundo que el COVID19 puede dejar tras de sí:Desde que comenzó la cuarentena, he ido a hacer mis compras permitidas en bicicleta (así hacía algo de deporte de camino; amén de que es más fácil aparcar). Pero la policía cada vez me paraba e interrogaba más y más preguntándome por los tickets de compra. Finalmente, creo que ya me tenían "localizado" o "fichado" de algún modo, me acusaron directamente de que iba en bici a comprar para hacer deporte (¡como si eso fuese delito!). Hace dos días me pidieron el DNI y amenazaron con multarme si me veían de nuevo en bicicleta siquiera para comprar el pan. Ayer vi que habían colocado un control policial a 50 metros de mi casa (cosa que no tiene sentido logístico alguno). Es evidente que me estaban esperando. Y es probable que incluso hayan usado drones y/o geolocalización móvil para el seguimiento de otros muchos ciclistas (mi caso no es el único ni mucho menos). Es más, en varias de las ocasiones que me pararon me hablaron de mala manera e incluso me insultaron a voces (intentando provocar una sobrereacción por mi parte; imagino que para poder justificar una multa con más base o para llevarme directamente al cuartel).Personalmente creo que esto que os cuento, que es un ejemplo muy local, se amplificará a nivel nacional y global. La tecnología al servicio de la censura y el acoso. Pérdida de libertades y retroceso político. Lo siento pero soy pesimista del mundo que va a dejar tras de sí el COVID19.
La OMS investiga a pacientes curados que vuelven a contagiarse
https://elpais.com/sociedad/2020-04-11/ultima-hora-del-coronavirus-en-espana-y-el-mundo-en-directo.htmlLa OMS investiga a pacientes curados que vuelven a contagiarse. La Organización Mundial de la Salud (OMS) está investigando a algunos pacientes con Covid-19 que dieron positivo nuevamente después de haber recibido el alta. Funcionarios surcoreanos informaron el viernes que 91 pacientes que creían curados habían dado positivo nuevamente. Jeong Eun-kyeong, director de los Centros para el Control y la Prevención de Enfermedades de Corea, dijo que el virus podría haber sido "reactivado" en vez de tratarse de una nueva infección. "Estamos al tanto de estos informes de personas que han resultado negativas para Covid-19 utilizando pruebas de PCR y después de unos días dan positivo de nuevo", ha dicho la OMS. Según las pautas de la OMS, un paciente puede ser dado de alta del hospital después de dos resultados negativos consecutivos con al menos 24 horas de diferencia en un paciente clínicamente recuperado. Según los estudios actuales, hay un período de aproximadamente dos semanas entre el inicio de los síntomas y la recuperación clínica de los pacientes con enfermedad leve por Covid-19. (Reuters)
"El coronavirus ha llegado para quedarse y no demos por seguro que habrá vacuna"(Francisco Salmerón)
Entrevista muy interesante. Dejo algunos extractos:La luz al final del coronavirus es el hallazgo de una vacuna, y nadie sabe más de vacunas en España que el doctor Francisco Salmerón. Empezó su carrera produciendo las de la gripe y la polio en los años setenta, en el Centro Nacional de Microbiología[....][...] Está convencido de que el SARS-Cov-2 ha llegado para quedarse y cambiará nuestras costumbres. Confía en que la comunidad científica logre una vacuna, pero advierte de que no se puede dar por hecho que vaya a conseguirse y que, incluso aunque se logre, podría tener una aplicación limitada. [...]P. ¿Qué ocurriría si quedara, ahora o dentro de unos meses, un 50% de la población por infectarse, por ejemplo?R. Pues que ese porcentaje se acabará infectando, inevitablemente. Es un virus muy infeccioso. Nunca he visto ninguno tan infeccioso como este. Y además, es muy peculiar, porque se está dando en todo el mundo. Se está difundiendo por países que están en invierno, en primavera y verano. Se está difundiendo a una velocidad pasmosa por todo el mundo. No olvidemos que hablamos de un virus que empezó hace cuatro meses.P. Con esos datos, ¿hay motivos para creer que el virus desaparecerá de España este verano?R. Por mi experiencia, creo que no. Es un visitante que ha llegado y se va a quedar.[...]P. La gran esperanza es el hallazgo cuanto antes de una vacuna. Hay muchas investigaciones en marcha, ¿será posible encontrarla?R. Se está dando por seguro que habrá vacuna, pero no crea que tener la voluntad de hacer una cosa es conseguirla. Cualquier compañía que hubiera hecho una vacuna frente al sida habría ganado muchísimo dinero. Y lo han intentado todas. No es una cuestión de invertir. Hay virus que se dejan más y otros que se dejan menos. El coronavirus es distinto del sida, pero tenemos que esperar. [...] No sabemos qué ocurrirá con el coronavirus. Con el sida, directamente no se ha conseguido, a pesar de haber hecho grandísimos esfuerzos. Se pusieron a trabajar en esa enfermedad los mejores virólogos, porque se percibió que era una enfermedad importante. Pero nadie fue capaz de sacar una vacuna, a pesar de que el interés era máximo.Noticia completa: https://www.elconfidencial.com/espana/2020-04-10/entrevista-francisco-salmeron-experto-vacunas-coronavirus_2542783/?fbclid=IwAR0Oe9UGKVX9VOMYoYBhmc10qFn_vuSiFLgDOVIJQhQjKOuakwDScteRJ5oRelacionado con: ¿Qué se sabe de la posible vacuna? (no hemos conseguido NUNCA una vacuna frente a los coronavirus)
Siguiendo en vivo y en directo el estado de los ensayos de vacunas para el COVID19
En esta web podemos estudiar el estado de los trials de cada tratamiento y vacuna que se encuentran actualmente en proceso de estudio para tratar el COVID19. Nos centraremos en el caso de la ansiada vacuna.La buena noticia.La buena noticia es que podemos ver en el listado que por el momento hay ya 6 vacunas que han comenzado, o van a comenzar en breve, la Fase I del proceso de ensayo (hay un ensayo más en proceso para el MERS, otro coronavirus activo que continua afectando a oriente medio).Esta Fase I consiste en ser una fase de la investigación que se centra en la seguridad de un medicamento (en este caso, la vacuna). Son pruebas que se realizan ya sobre humanos, una vez el medicamento ha sido probado con éxito en animales y/o in vitro. Por lo general, se realizan con voluntarios sanos y el objetivo es determinar los eventos adversos más frecuentes y graves del medicamento y, a menudo, cómo el cuerpo descompone y excreta el medicamento. Estos ensayos generalmente involucran a un pequeño número de participantes. Entre 20-80 personas. La duración media de esta fase de estudio es de 12 meses.Así pues, si entramos en uno de los ensayos, por ejemplo el primero, nos encontramos lo siguiente: https://clinicaltrials.gov/ct2/show/NCT04283461?term=Cov-2&cond=Vaccine&phase=01234&draw=2&rank=1Harán la primera fase con 45 participantes sanos utilizando lo que han dado en llamar: ARNm-1273, una nueva vacuna basada en ARNm encapsulada en nanopartículas lipídicas (LNP) que codifica una proteína de espiga (S) estabilizada por prefusión de longitud completa de SARS-CoV-2 (el virus que causa la enfermedad del COVID19). Se hará una prueba dividiendo los 45 participantes en subgrupos y a cada cual se le dará una dosis diferente, aunque siempre por inyección intravenosa.En el apartado que dice Outcome Measures se puede ver qué resultados pretenden medir del estudio para descartar o aprobar el paso a la Fase II.El fin del estudio de la Fase I de esta vacuna en concreto está programada para el 1 de junio del 2021. En ese momento se habrán estudiado por completo a los 45 participantes, y se verá si los resultados obtenidos, en relación a las expectativas (Outcome Measures); permiten o no (descarte) el pase de este medicamento a la siguiente Fase II.La mala noticia.Y ahora viene la "mala" noticia (que es mala simplemente porque no es conveniente, no porque sea un procedimiento mal diseñado):La estadística dice que de media el 70% de ensayos suelen pasar la Fase I, mientras que el 30% restante se rechaza. Como aproximación se podría decir que, con suerte (quitando la vacuna en pruebas para el MERS), a mediados del año que viene tendremos aproximadamente unas 3-4 vacunas dispuestas para comenzar la Fase II.Esta Fase II es una fase de investigación para describir ensayos clínicos que recopilan datos preliminares sobre si un medicamento funciona en personas que tienen una determinada afección / enfermedad (es decir, la efectividad del medicamento). Por ejemplo, los participantes que reciben el medicamento pueden compararse con participantes similares que reciben un tratamiento diferente, generalmente una sustancia inactiva (llamada placebo) o un medicamento diferente. La seguridad continúa siendo evaluada y se estudian los eventos adversos a corto plazo. Este ensayo se realiza sobre un grupo de entre 100-300 personas.La duración de la segunda fase suele estar de media entre 12-48 meses (en ocasiones más tiempo). La estadística dice que "sólo" un 33% de los medicamentos pasan esta segunda fase, quedando el resto descartado principalmente debido a baja eficiencia, graves efectos secundarios, o a importantes contraindicaciones con otros medicamentos, o con patologías preexistentes de los pacientes.De este modo, con suerte, a mediados del 2022 tendremos entre 1-2 vacunas listas para pasar a la Fase III.La Fase III es una fase de investigación para describir ensayos clínicos que recopilan más información sobre la seguridad y efectividad de un medicamento mediante el estudio de diferentes poblaciones y diferentes dosis y al usar el medicamento en combinación con otros medicamentos. Estos estudios generalmente involucran a más participantes. En concreto, entre 1000-3000 personas.La duración media de esta tercera fase también suele ser de 12 meses. Y "únicamente" entre un 25%-30% pasan a la Fase IV (o directamente a producción si se opta por obviar este paso). El resto debe ser descartado por los mismos motivos que en la fase anterior una vez la diversidad de la muestra fue mucho mayor.Por lo tanto, y si se siguen el estándar actual de seguridad, para mediados del 2023 tendremos entre 0-1 vacuna lista para pasar a producción y distribución (la probabilidad de tener 1 vacuna para esa fecha, si ya tuvimos la suerte de pasar las dos cribas anteriores con algún candidato restante, es no obstante bastante baja ~30%).Descarto que se vayan a permitir el lujo de realizar la Fase IV de revisión y aprobación final, así que me la salto y no la tengo en cuenta.Fabricación y distribución.Por lo tanto, tras la Fase III, si fuimos afortunados, finalmente pasaremos al "problema" de la fabricación y distribución de la vacuna: no todas las vacunas son igualmente fáciles de producir (algunas permiten producir millones de dosis a la semana, otras únicamente cientos de miles, etc.); lo mismo que algunas son más caras que otras (según el equipo y la tecnología necesaria y su disponibilidad mundial). Si a mediados del 2023 contamos ya con un candidato aprobado, habrá que ver cómo de eficaz es a la hora de ser fabricado en masa y distribuido luego a los 7.000 millones de personas del planeta.No es descabellado encontrarnos con el contratiempo añadido de requerir al menos otro año más de demora hasta que esa posible vacuna llegue a cada rincón del mundo.Por lo tanto, y si no nos saltamos ahora por las buenas el sistema de ensayo médico de seguridad para nuevos medicamentos (utilizado desde mediados del siglo pasado); es probable que, como ocurre normalmente, una vacuna/tratamiento para el COVID19 no esté disponible para toda la población aproximadamente hasta mediados del 2024. A cuatro años vista.En resumen.La estadística general de ensayos nos dice que los nuevos medicamentos tardan de media entre 5-9 años en estar disponibles para su comercialización, por lo que esos cuatro años vista de los que hemos hablado antes es un dato incluso bastante optimista: y lo que nos venden por televisión de los 12-18 meses es simplemente mentira. Ya sólo la Fase I hemos visto que dura de media 12 meses, y saltarse los protocolos de seguridad sería proceder de manera suicida. Imaginad que, por acelerar, se unen en una la Fase II y la Fase III, es decir; que se pasa de probar sobre 80 personas a probar directamente sobre 3000 (saltando el paso previo sobre 100-300). Si resulta que la medicación contiene implícita una contraindicación mortal (cosa que no es para nada descartable) que por mala fortuna escapa del control inicial sobre 80 individuos, podríamos llegar literalmente a matar a miles de personas al pasarse directamente de la Fase I a la Fase III donde la diversidad de individuos es mucho mayor y heterogénea.No creo que nadie (ni organización privada ni pública) se arriesgue y sea tan irresponsable, la verdad.







Falseando datos. Y luego criticábamos a China e Irán por lo mismo. Si es que es lógico. Con el tiempo lo harán todos los países porque no hay economía que aguante la verdad. En fin. Es lo que nos ha tocado, aprender a convivir con el dichoso virus mientras no llegue la vacuna.